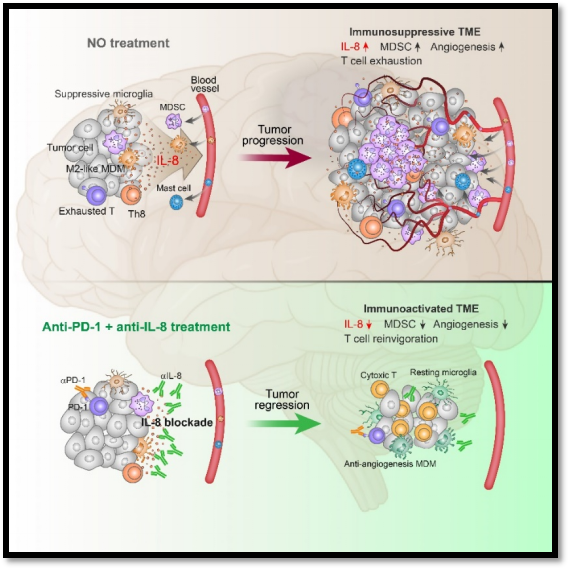
脑胶质瘤是最为常见的中枢神经系统原发肿瘤。肿瘤发生的特殊位置及其侵袭生长的特性,导致脑胶质瘤很难通过手术完全切除。高级别胶质瘤的复发率几乎为100%,平均生存时间仅为14个月【1】。近年来,免疫检查点阻断(Immune checkpoint blockade,ICB)取得突破性进展,已成功用于治疗多种类型的肿瘤,但其对脑胶质瘤的治疗效果并不理想。以MDSC大量浸润、促肿瘤的TAM分化和血管异常增生为特点的免疫抑制微环境是肿瘤形成对ICB治疗抵抗的关键因素【2】。为提高脑胶质瘤的免疫治疗效果,我们需要深入了解脑胶质瘤中T细胞的功能、状态及其免疫抑制微环境的形成机制。2023年3月23日,来自陆军军医大学第一附属医院的刘新东、卞修武、王岩团队和第二附属医院的吕胜青团队在Cancer Cell上在线发表题为 Neutralizing IL-8 potentiates immune checkpoint blockade efficacy for glioma 的文章,揭示了IL-8在构筑脑胶质瘤免疫抑制微环境中的作用及作为免疫治疗靶点的潜在应用价值,为脑胶质瘤的免疫治疗提供了新的见解。肿瘤浸润T细胞的功能状态是决定抗肿瘤免疫应答和免疫治疗响应的关键因素。在多数情况下,肿瘤浸润T细胞越多提示抗肿瘤免疫应答水平越强。然而,胶质瘤微环境中的T细胞含量随着肿瘤等级的升高而升高,提示胶质瘤T细胞功能的多样性。最新的研究表明,脑胶质瘤中发生克隆扩增的肿瘤特异性T细胞主要包括耗竭、效应和记忆三种亚群【3】,然而肿瘤中其余非克隆扩展的T细胞的功能尚不清楚。本文研究人员首先通过组织学分析了脑胶质瘤中T细胞的分布,发现T细胞主要分布在血管周,基于Ivy GAP数据库的分析也证明了这一结论。为进一步探究介导T细胞向肿瘤组织迁移的趋化因子受体,作者利用质谱流式(CyTOF)比较分析了脑胶质瘤病人外周血和肿瘤组织中趋化因子受体的表达情况,发现肿瘤浸润T细胞高表达趋化因子受体CCR5和CXCR3,提示这两种受体参与介导T细胞向肿瘤的迁移。为了系统的分析肿瘤微环境中T细胞的功能状态,作者对脑胶质瘤病人血液和肿瘤的T细胞进行了单细胞测序并比较分析,发现肿瘤浸润T细胞包含了18个亚群包含了7个CD4+ T细胞亚群、10个CD8 T细胞亚群以及一个γδ T细胞亚群。值得注意的是,作者在肿瘤CD4+ T细胞中发现了一个高表达IL-8的亚群(Th8)。Th8的TCR克隆水平低,提示为非肿瘤特异性T 细胞,高表达IL8、IL1B、CCL3等分泌性因子以及转录因子BHLHE41,并与病人生存负相关。鉴于Th8只存在于肿瘤组织中,作者推测肿瘤细胞分泌的因子诱导Th8的形成。为验证这一猜想,作者用脑胶质瘤肿瘤原代细胞培养上清诱导健康人初始CD4+ T细胞,发现肿瘤细胞培养上清能够诱导T细胞释放IL-8,并且经过肿瘤上清诱导的T细胞和体内的Th8细胞具有相似的转录谱特征,表现出先天性免疫细胞的特性。通过体内外试验,作者证明肿瘤上清诱导的T细胞具有募集髓系抑制细胞(MDSC)和促进血管形成的能力。为了进一步探究Th8细胞分化形成的内在调控机制,作者在T细胞中过表达了一系列转录因子,结果显示过表达BHLHE41能够强烈的诱导T细胞表达IL-8,后续的功能实验表明过表达BHLHE41的T细胞具有类似Th8的特征。然而当作者利用Crispr-cas9敲除BHLHE41时,并没有发现IL-8的下调,这说明BHLHE41是CD4+ T细胞表达IL-8的充分非必要条件。临床上,血清IL-8水平与病人肿瘤负荷正相关,与ICB治疗效果负相关【4,5】。然而由于啮齿动物基因组中不含有IL8基因,IL-8在肿瘤发生过程中的免疫调节功能尚不清楚。为在体内探究IL-8的免疫调节功能,作者构建了IL-8全人源化小鼠(IL8-Hu)。脑胶质瘤在IL8-Hu小鼠体内的生长速度更快,肿瘤组织中含有更多的MDSC,且具有与临床样本相似的病理组织学特征。anti-PD-1单药治疗不能抑制肿瘤在IL8-Hu小鼠上的生长。进一步研究发现,PD-1阻断治疗使肿瘤组织和血清中IL-8水平升高,导致肿瘤组织中MDSC浸润增多。这一现象驱使作者进行IL-8和PD-1的联合阻断治疗。与预期相符,IL-8和PD-1的联合治疗几乎阻断了MDSC向肿瘤的募集,抑制肿瘤血管新生,降低T细胞耗竭,显著延长小鼠生存期。为更加全面的探究IL-8阻断治疗对肿瘤免疫微环境的影响。作者对不同处理的小鼠进行了单细胞测序分析。与前期的发现一致,阻断IL-8后肿瘤中的MDSC显著减少。通过对单核细胞源巨噬细胞(MDM)和小胶质细胞的聚类分析,作者发现阻断IL-8后肿瘤中M2型巨噬细胞和免疫抑制性小胶质明显减少,而抗血管生成MDM增多。这说明阻断IL-8改变了巨噬细胞和小胶质细胞的分化轨迹,逆转了肿瘤免疫抑制微环境。综上所述,本文利用多组学的研究手段揭示了脑胶质瘤中T细胞的分布特点和功能特征。发现并鉴定了一群高表达IL-8的CD4+ T细胞(Th8)。Th8细胞通过释放IL-8,与肿瘤细胞和髓系细胞一道构筑肿瘤免疫抑制微环境。阻断IL-8能够逆转肿瘤的免疫抑制微环境,增强免疫检查点阻断的治疗效果(图1)。陆军军医大学第一附属医院、金凤实验室刘新东教授、卞修武院士、王岩教授和陆军军医大学第二附属医院吕胜青教授为论文共同通讯作者。陆军军医大学第一附属医院、金凤实验室的刘浩飞博士为第一作者。https://doi.org/10.1016/j.ccell.2023.03.004
1 Lim, M., Xia, Y., Bettegowda, C. & Weller, M. Current state of immunotherapy for glioblastoma. Nat Rev Clin Oncol 15, 422-442 (2018). https://doi.org:10.1038/s41571-018-0003-5
2 Morad, G., Helmink, B. A., Sharma, P. & Wargo, J. A. Hallmarks of response, resistance, and toxicity to immune checkpoint blockade. Cell 184, 5309-5337 (2021). https://doi.org:10.1016/j.cell.2021.09.020
3 Mathewson, N. D. et al. Inhibitory CD161 receptor identified in glioma-infiltrating T cells by single-cell analysis. Cell 184, 1281-+ (2021). https://doi.org:10.1016/j.cell.2021.01.022
4 Yuen, K. C. et al. High systemic and tumor-associated IL-8 correlates with reduced clinical benefit of PD-L1 blockade. Nat Med 26, 693-698 (2020). https://doi.org:10.1038/s41591-020-0860-1
5 Schalper, K. A. et al. Elevated serum interleukin-8 is associated with enhanced intratumor neutrophils and reduced clinical benefit of immune-checkpoint inhibitors. Nature Medicine 26, 688-+ (2020). https://doi.org:10.1038/s41591-020-0856-x