早在2018年,上海市第六人民医院的胡承教授和贾伟平教授就在期刊《Diabetes》上发表了有关“中国糖尿病流行病学”的综述。

(https://doi.org/10.2337/dbi17-0013)

规范地制作糖尿病动物模型是研究糖尿病疾病机制和防治方法的第一步。
如何才能更好地在动物身上模拟出糖尿病的各种疾病表现呢?
01 —
糖尿病背景
(写这一部分,并不是为了无端地扩充本文体量,而是后面介绍动物模型时,将根据此部分内容分类描述。因此,这一部分主要起到一定地铺垫作用。)
糖尿病是由多种疾病因素复合导致的以慢性血糖水平增高为特征的全身慢性代谢性疾病,与家族遗传、环境因素以及自身免疫相关,具体的发病机制目前尚未完全阐明。
糖尿病的典型表现是空腹血糖≥7.1mmol/L或者任意时刻血糖≥11.1mmol/L,再结合相应的临床症状(三多一少)即可诊断。这些大家都十分清楚。
糖尿病还会导致糖尿病心脏病、糖尿病肾病、糖尿病视网膜损害、糖尿病神经损害、糖尿病继发的伤口不愈合及感染等等。这些都是值得关注和研究的内容。
糖尿病分型:主要分为1型糖尿病(胰岛素绝对缺乏)、2型糖尿病(胰岛素进行性分泌不足或抵抗)、妊娠期糖尿病和特殊类型的糖尿病4种。目前临床上主要见到的就是前两种,因此下面介绍的动物模型主要围绕这两种类型而展开。
02 —
1型糖尿病动物模型
一般而言,1型糖尿病发病人数占临床确诊糖尿病总人数的10%左右。
典型的表现就是胰岛β细胞被破坏,导致胰岛素绝对缺乏,从而引起高血糖等全身性的代谢障碍。
目前使用较多的动物模型主要有3种。
2.1 STZ诱发的糖尿病动物模型
STZ全称链脲佐菌素,这种药物的亚硝基脲结构能够选择性地损伤胰岛β细胞,损伤后的胰岛重构,继而纤维化。显然,STZ的剂量是关键因素,注射剂量大则完全损伤胰岛,胰岛素绝对缺乏,形成1型糖尿病。
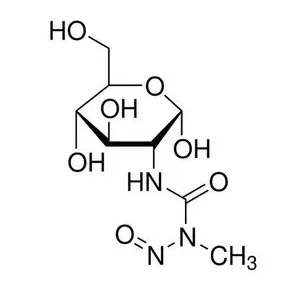
大鼠需要禁食不禁水12h,尽可能使用雄性,因为雌性对STZ的反应并不均一,这可能与雌激素水平有关。STZ一般是现用现配2%浓度,采用单次腹腔注射即可,注射量50mg/kg(一定要注意回抽,严格禁止注入胃肠道)。
注射STZ溶液2天或者3天后,连续3天采用尿糖检测试纸检测尿糖水平,血糖水平采用葡萄糖氧化酶法检测即可,若尿糖≥3+,血糖持续升高,说明注射是没问题。一周后大鼠可出现三多一少症状,再次检测,若尿糖≥3+,血糖≥16.67mmol/L,说明造模成功。
注意事项:
(1)尽量不用小鼠,因为小鼠对STZ敏感度不高,容易造成组内差异较大。
(2)上面提到的血糖、尿糖指标以及测定时间是比较很多资料后得出的,公认性也较强,是可用的。
(3)单次大剂量注射才是可取的,小剂量只会造成胰岛炎。
(4)血糖越高,动物死亡率越高,因此要严格控制STZ的注射剂量,预实验摸索条件是必须的;可以适当的补充胰岛素,防止低血糖导致的大量动物死亡。
(5)STZ造模比较适合长期观察,因为这种药物导致的胰岛损伤不易修复,大鼠不易代偿。
(6)静脉注射的死亡率比腹腔注射高。
2.2 allxon诱发的糖尿病动物模型
allxon全称四氧嘧啶,它也是一种细胞毒物质,可以通过超氧自由基破坏胰岛β细胞,使得胰岛素分泌减少。一般配成1%-3%浓度即可使用。注射剂量为30-40mg/kg,静脉注射效果较腹腔注射要好。
一个需要注意的问题是allxon的注射速度。有人研究过,30s快速静推的成模率比缓慢注射要高。
动物呢,还是尽可能全部选用雄性,造模前禁食不禁水12h。这样可以增大动物对allxon的敏感性。

注射之后6小时,采用25%葡萄糖水灌胃可以显著地减少动物死亡率。注射后18h,大鼠即可出现高血糖、多尿、多饮等典型症状,血糖会升高至16.67mmol/L以上。随着时间的推移,2周左右即可形成1型糖尿病模型。
注意事项:
(1)很多研究都显示,注射allxon一个月之后,部分大鼠的血糖会恢复至正常水平,这可能是由于大鼠胰岛代偿作用导致的。这样分析的话,allxon造出的模型可能更加适合短期观察。
(2)不要用豚鼠,豚鼠对allxon不感冒,甚至还有抵抗作用。
(3)STZ比allxon贵好多钱。
2.3 自发性1型糖尿病动物模型
(1)BB大鼠
BB大鼠在早期常表现胰岛炎症,但是晚期多发生严重的胰岛纤维化。
(2)NOD小鼠
NOD小鼠并不是出生就有糖尿病,而是在100-200日龄时突然发生糖尿病的一种啮齿类动物,并且雌性发病率更高。它的发病机制可能与免疫介导的胰岛炎症有关。
小编认为此模型的好处是补充了其它模型的短板。因为其它的模型都是更常用雄性。一个客观的事实是临床上糖尿病女性病人也不少。NOD小鼠为咱们研究雌性1型糖尿病的发病机制提供了一个窗口。
03 —
2型糖尿病动物模型
3.1 高脂高糖饮食加STZ大鼠动物模型
前面说了,STZ可以选择性破坏胰岛细胞,且破坏程度与STZ的用量有关。
这种模型就是先给大鼠喂高脂高糖饲料,以诱发胰岛素抵抗,随后再腹腔注射小剂量的STZ不完全损伤胰岛β细胞,以诱发分泌障碍;最终就造成了大鼠2型糖尿病。
一直以来,使用高脂高糖饲料造模的各种动物模型,饲料的配方比较关键,大家也比较关注这个问题。可以买商用的饲料,但是有点贵。如果自己配制,可以参考以下配方,该配方来自《人类疾病动物模型的复制》第2版。
“猪油10%,2.5%胆固醇,20%蔗糖,1%胆酸盐,66.5%普通饲料。”
造模很简单。高脂高糖饲料喂4周;然后25mg/kg的剂量注射STZ(浓度为0.25%),接着继续高脂高糖饲料喂养4周。也可以将STZ剂量提高到30,每周1次,连续2周。都是可行的。
验证模型的标准是血糖大于7.8以及胰岛素敏感指数下降。
注意事项:
(1)高脂高糖饮食的动物非常容易死亡,尤其是在注射了STZ之后依然采用高质高糖喂养,这个死亡率真的说不准。
(2)糖尿病动物极易发生感染,动物间的撕咬伤也不易愈合;此外要经常换垫料,因为动物都是多尿的,潮湿的饲养笼更容易出问题。唯一的办法就是勤快点,细心照料你的动物。
3.2 自发性2型糖尿病动物模型
科研同道们,这里面可有得聊了。
(1)KK-A(y)小鼠
这是具有黄色肥胖基因的KK小鼠。KK小鼠是日本学者培育的一种轻度肥胖型2型糖尿病小鼠,之后与C57BL/6J小鼠杂交,近亲繁殖后得到KK-A(y)小鼠。这种小鼠在5周左右就出现了肥胖和糖尿病症状,胰岛细胞随之经历了脱颗粒和糖原变性、肥大和空泡化、脂肪变。
值得注意的是,KK-A(y)小鼠在很早期的时候就会出现糖尿病肾病表现,基底膜增厚明显,进展很快。小编觉得KK-A(y)小鼠是研究糖尿病肾病的一个很好的模型。下面还要再介绍另外一个糖肾模型哦。
(2)ZDF大鼠
其实说白了ZDF大鼠就是从Zucker大鼠中得到的。一些Zucker大鼠天生有胰岛素抵抗,有人就把这些动物拿来近亲繁殖,最终获得稳定遗传的ZDF大鼠,ZDF大鼠的血糖一般不高,但是其血浆甘油三酯游离脂肪酸水平很高。这些均匀fa基因有关。
有关ZDF大鼠胰岛病变特征的详细资料可以查阅以下3篇文献,说的很详细,感兴趣的可以百度一下,写的很好。
① “Morphology of pancreatic islet: a time course of pre-diabates in zucker fatty rats.”
② "Variation in characteristics of islets of langerhans in inslin-resistant, diabetic and non-diabatic-rat strains."
③ "Diabetes in Zucker Fatty Rat."
(3)db/db小鼠
这个就比较常见了。这种小鼠是从C57BL/KsJ中筛选出的自发性糖尿病小鼠。

小鼠出生后就开始贪吃,然后就胖成了上图那样。随后出现出现典型的三多一少,一般活不过10个月,大多死于酮症。(贪吃的后果啊!)
最值得注意的是小鼠出生2个月就有糖肾表现,是国际公认糖肾动物模型。这一点是采用普通大鼠造模很难达到的一点,普通大鼠造模后饲养很久很久有时都难以看到典型的肾病表现,就更不谈糖尿病心肌病或者糖尿病视网膜损伤了。有研究显示,如果想得到糖尿病眼底病变动物模型,采用传统方法,动物起码需要养2年,养完就毕业了。
(4)ob/ob小鼠
ob/ob小鼠是典型的肥胖+高血糖小鼠。为啥叫ob/ob呢?就是胖的(obese)。
这种小鼠在早期即可出现自发的高血糖、糖尿、高胰岛素血症。不禁食的情况下,血糖基本上都是高于16.67的。国内外使用的较多。
(5)其它动物模型
04 —
验模指标
(1)禁食空腹血糖检测
(2)口服葡萄糖耐量试验
(3)血胰岛素水平
(4)胰岛素敏感指数














