一 流式基础介绍
01 原理 流式细胞术(Flow Cytometry, FC)利用流式细胞仪可以快速定量分析细胞群(或微粒)的物理化学特征,以及根据这些物理化学特征进行精确分选。 02 流式细胞仪的基本结构
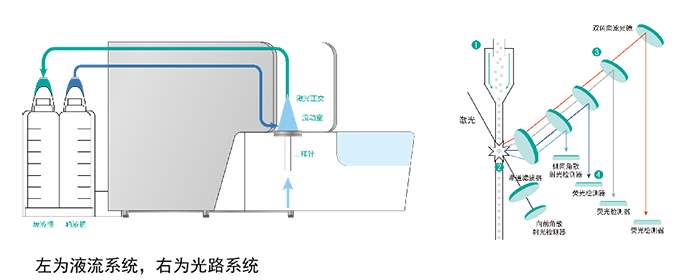
流式细胞仪主要是由液流系统、光学系统、电子系统构成(部分机型还包含细胞分选系统)。
其中液流系统的作用是让细胞能够单列排列依次通过光信号检测点,是光路系统发挥作用的基础;
光路系统始于激光器发射器,发射不同波长激光照射到细胞后,产生的光信号(散射光信号和荧光信号)会经过不同光学滤片传输到不同通道探测器;
电子系统负责将接收到的光学信号转化为电子信号并进行分析,从混合细胞群中鉴别出不同的亚群;而具有分选功能的流式细胞仪则还能从大量细胞中分选出感兴趣的亚群进行更多研究。
因此通过流式细胞仪,我们可以对液体中的悬浮细胞进行快速定量分析和分选。
03 流式图片
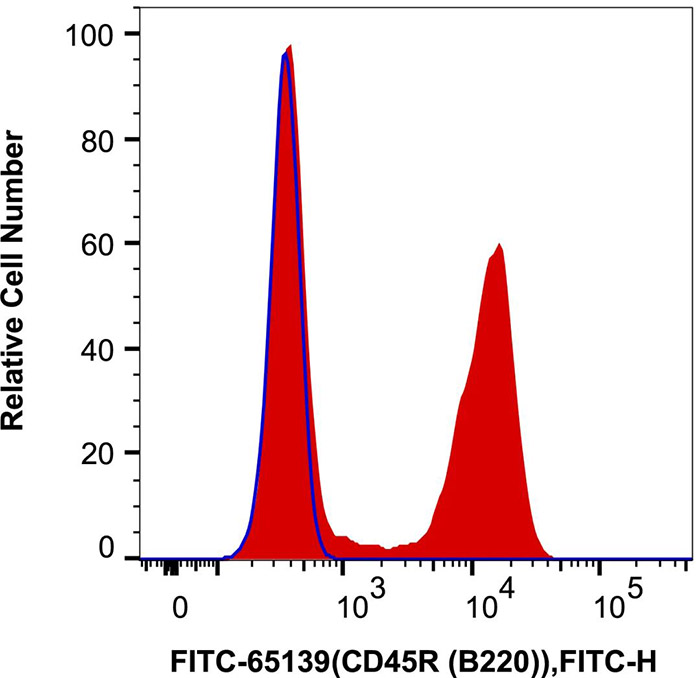
1. 直方图
x轴代表一个通道的值,反映荧光信号或散射光信号相对强度,通常为对数,也可以为线性。y轴一般是细胞数。
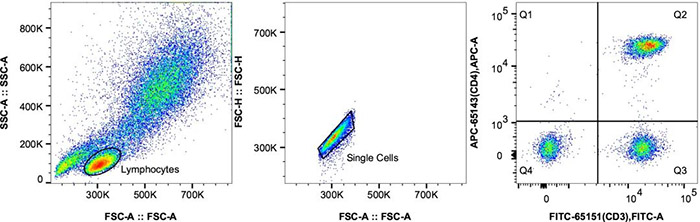
2. 散点图
x和y轴分别代表一个通道的值,反映荧光信号或散射光信号相对强度。通过两个参数可以将细胞亚群分开。
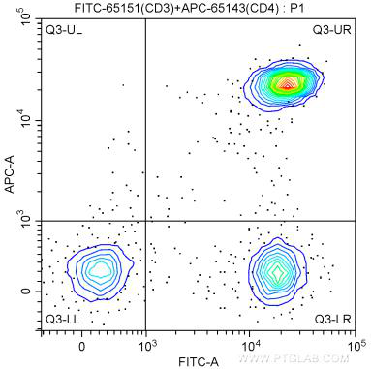
3. 等高线图
借助地理的等高线图表示细胞的密集程度,环线代表密度相同的区域,环线中央代表细胞聚集的中心。
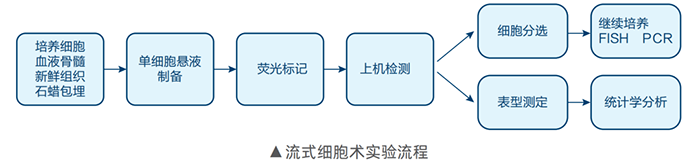
二 流式基本操作及技巧 01 常见样本的流式检测步骤
◆ 常规单细胞流式检测步骤 ⇩滑动查看全部 1. 制备单细胞悬液:贴壁细胞可用胰酶消化成单细胞后收集于离心管中,悬浮细胞可直接收集,离心 (2000 r,5 min) 去除残留培养基,1xPBS离心洗涤1-2次后,1xPBS 重悬沉淀制成单细胞悬液。 2. 离心沉淀细胞并去除上清液,按每 1x106个细胞大约 100 μl 固定剂的密度重悬细胞,室温下 (20-25℃) 固定约 20 min。 3. 离心 (3000 r,5 min) 去除固定剂,使用通透剂洗涤两遍。(若通透剂通透效果过程可逆则通透剂需一直存在) 4. 按每 1x106 个细胞大约 100 μl 通透剂的密度重悬细胞,静置 10 min。 5. 在每 100 μl 细胞重悬液中,4℃避光孵育直标偶联抗体 45-60 min,抗体的使用浓度根据建议或者滴定结果。(直接标记法可以进入第 9 步)。 6. 若使用间接标记法,一抗孵育步骤与步骤 5 一致。 7. 离心沉淀细胞并丢弃上清液,重复操作。 8.加入150 μl 稀释好的荧光物质偶联的二抗(二抗稀释度使用建议浓度)重悬细胞,4℃避光孵育 45-60 min。 9. 洗涤,离心沉淀细胞,丢弃上清液。200 μl 通透剂重悬细胞,并在流式细胞分析仪上进行分析。 ◆ 人外周血细胞表面抗原的流式检测步骤 ⇩滑动查看全部 1. 在每个 2 mL EP 管或流式检测管中加入 100 μl 全血。 2. 按照抗体说明书中指定条件加入抗体后,轻轻混匀。 3. 避光室温孵育 15-30 min。 4. 裂解红细胞之前,应使裂解液平衡至室温。 5. 将待裂解全血轻轻混匀后,每 100 μl 全血加入适量裂解液立即在涡旋仪上震荡 1 s。(推荐使用 Proteintech 红细胞裂解液,货号: PF00014/PF00015) 6. 室温下避光裂解 10 min 左右。 7. 加入 1xPBS至2 ml终止裂解。 8. 室温下 300-400 g 离心 5 min,弃红色上清。 9. 加入 2 ml PBS 颠倒混匀后,室温下 300-400 g 离心 5 min,弃上清。 10. 加入 200 μl PBS 混匀后,尽快上机检测。 ◆ 人外周血细胞表面抗原检测注意事项 ⇩滑动查看全部 1. 结合能力较弱的抗体可以适当延长孵育时间,建议进行预实验。 2. 血液样本个体差异较大,裂解时间可能会有细微变化。如果全血红细胞含量较高,可以用适量的 PBS 稀释全血。 3. 当孵育完抗体后,有可能红细胞会沉淀在底部,没有混匀的话可能会导致裂红不充分。 4. 裂解方法可以根据实际情况进行调整,适当增减工作液体积或裂解时间均可。 5. 用裸眼评估裂解效果,如果外观浑浊或者光散射直方图异常,可能为裂解不完全。 6. 若使用不含固定剂的裂解液裂解红细胞后,完成实验后不能立即上机检测时,可以用固定剂固定细胞后再上机检测。防止放置时间过长细胞死亡导致细胞分群较差。(固定剂 1%-4% 多聚甲醛均可。) 7. 若使用的一抗不是标记荧光抗体,则在上述检测步骤9后加入适量的二抗稀释液。避光孵育 15-30 min。重复上述步骤9洗涤细胞 1-2 次后,进行上述步骤10。 8. 若要对多个细胞表面抗原进行多色标记时,可以同时加入荧光标记抗体后按照以上步骤进行孵育和细胞洗涤。实验操作尽量保持在避光的条件下进行,防止荧光淬灭。 ◆ 小鼠脾组织细胞(表面&核内胞内)流式检测步骤 ⇩滑动查看全部 1.样本制备 a. 取材:利用急性大失血法将小鼠处死,泡在75%的酒精中 5 min后,放入超净台,取出小鼠脾脏,置于平皿中,放冰上。 注意:摘眼球法将小鼠处死时,要尽量将血液放干净,防止在制样时红细胞过多,离心弃上清后,细胞聚团无法吹散导致样本的损失较大。 b. 用PBS缓冲液洗涤,并且剔除脾脏周围脂肪,结缔组织等。 c. 利用钢网研磨法:将洗净的脾脏放置不锈钢网(200目) 上,用注射器针芯或用弯头组织镊子轻轻研压脾脏,获取细胞悬液。 d. 研压完毕后,用细胞筛网过滤悬液两次。以除去未研压充分的组织。 e. 将过滤后的悬液 300-400 g,离心 5-10 min,弃上清。 f. PBS缓冲液5mL,轻轻冲散细胞,再离心一次,弃上清。 g. 每管视细胞量加入红细胞裂解液 1-3 ml,冰上孵育 10-15 min 后直接离心。 注意:裂解红细胞时,时间不宜过长以免破坏其他细胞。如果需要继续培养和诱导分化的,不建议裂红。 h. 视细胞量加入 1-2 ml PBS。取小样,台盼蓝染色后,用血球计数板计数。 i. 将细胞调整到 107/ml 左右,分在 5 ml EP管或者流式检测管中。 2.细胞表面染色 a. 每个 2 ml EP 管内分别加入 100 ul 细胞悬浮液,加入表型抗体,涡旋混匀,4℃孵育 15-30 min。 b. 加入 2 ml PBS 洗涤,400-500 g 离心 5 min,弃上清,洗涤 2-3 次。 c. 加入 200 μl PBS 重悬细胞后,上机检测。( 有荧光抗体存在的情况下注意避光操作 ) 注意:若来不及进行检测,可以加入固定剂后 4℃过夜(固定剂 1%-4% 多聚甲醛均可)。建议尽快上机检测以防止信号减弱或固定剂对某些荧光素或蛋白的影响。 3.细胞核内染色(胞内染色) a. 先根据需要对细胞表面标记进行染色,步骤如上。 b. 最后一次洗涤完后,弃上清。保留残余体积,大概 100 μl 左右涡旋仪上涡旋细胞使沉淀完全解离。 c. 向每个管中加入适量的 Foxp3 固定 / 破膜试剂盒的固定工作溶液并涡旋细胞混匀。 d. 在室温下避光孵育 30-60 min。 e. 每管加入 2 ml 1X 破膜液,在室温下 400-600g 离心 5 min,弃上清。 f.( 可选 ) 重复第 5 步。 g. 加入 100 μl 1X 破膜液重悬细胞,不洗涤,加入推荐量的荧光标记抗体以检测核内抗原,并在 4℃避光孵育 45 min。 h. 每管加 2 ml 1X 破膜液,在室温下 400-600g 离心 5 min,弃上清。 i. 重复步骤 8。 j. 加入 200 μl PBS 重悬细胞后,上机检测。
02 荧光素的选择
荧光素是一类光反应物质,能吸收特定波长的光能,并发出更长波长的光线,即荧光。
激发光谱(吸收光谱):能特异性激发某种荧光素的一定范围内光线。
发射光谱:激发光激发荧光素使其发射的一定波长范围内的光。
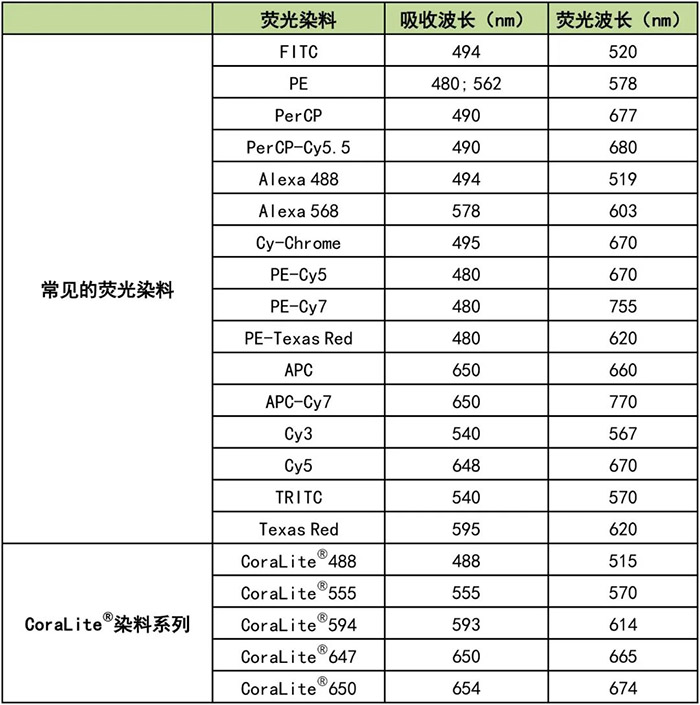
★ CoraLite®是Proteintech公司自有的具有良好光稳定性、发光强度以及较宽pH适应性,能完美胜任科研实验要求的染料系列。
◆ 荧光染料选用的特性
a. 串联荧光素:Percp-Cy5.5、PE-Cy7、APC-Cy7 等,对光稳定性差,固定破膜后易断裂,Cy 系列为花青素染料,极易结合死细胞,或造成非特异性着色;
b. FITC 对较低的 pH 敏感;
c. 避免使用冻融后的单标。
◆ 根据抗原表达强弱合理选择荧光素
a. 高表达的抗原可以根据实验需求选用合适的流式荧光抗体,低表达抗原一般需要用较亮的荧光素检测;
b. 多色搭配时,亮度高的荧光素用于低表达的蛋白,亮度弱的用于高表达蛋白;
c. 如果对所检测的抗原表达量不清楚,对于Panel内重要的抗原选择最强的荧光素。
常用荧光的强弱如下:
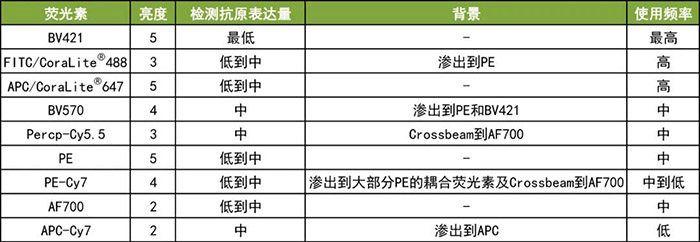
03 设置对照
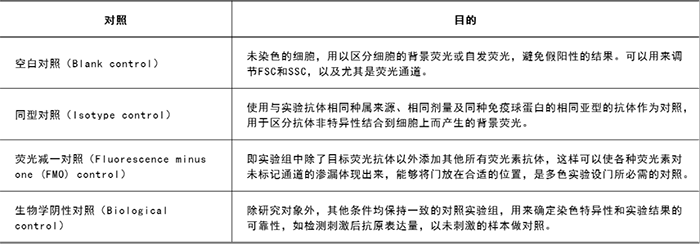
设置合理的对照组是整个流式实验成功的关键,流式对照至少有 4 种:空白对照,同型对照,荧光减一对照和生物学对照,主要目的是为了避免出现假阳性或假阴性结果。(点击下表查看大图)
三 流式疑难解析 流式的常见问题,可以点击放大查看原图哦 四 流式案例解答