在最近一个世纪,小鼠被广泛应用于生物学研究,并作为癌症模型为癌症治疗的进步做出了重大贡献。
癌症模型的评估和分类使科学家对肿瘤的潜在遗传机制有了深入的了解,具有临床预测特性的小鼠动物模型可将候选药物从临床前阶段推进到临床阶段。
今天我们重点介绍“PDX”模型。
一、什么是PDX模型?
PDX为Patient-Derived Tumor Xenograft,人源性肿瘤组织异种移植模型,是指将来源于患者的肿瘤组织植入免疫缺陷小鼠体内,从而建立的移植瘤模型。
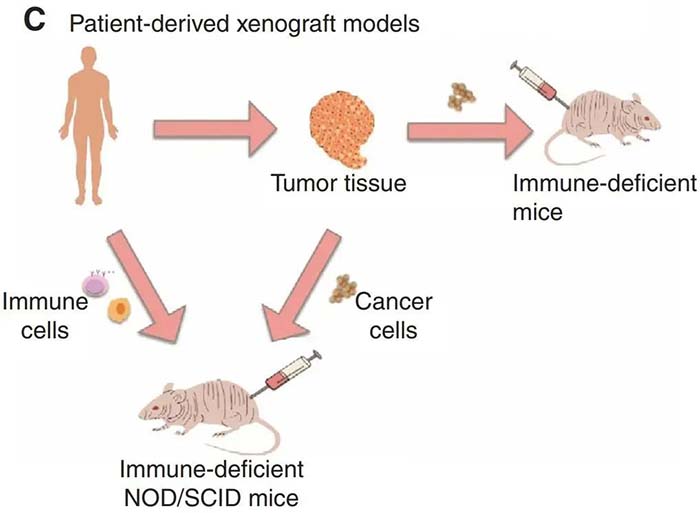
(DOI: 10.1158/2159-8290.CD-18-0044)
与CDX模型的区别 CDX为cell-line derived xenograft,是细胞系来源的异种移植模型,是指将人体肿瘤细胞在体外(培养皿中)筛选,经过传代培养建立的稳定的细胞株,然后再注射到免疫缺陷的小鼠体内建立模型。 与稍早建立的直接来源于患者的PDX模型相比,CDX模型的细胞系容易获得,建模难度低,且有大量关于其细胞功能、药理药效等的文献数据可供参考,整体的成本低,一度成为各大实验室的主流方法。 但在2016年,美国国家癌症研究所(National Cancer Institute,NCI)宣布NCI-60细胞系退役,NCI60细胞退出药物筛选系统时已使用了25年,这意味着CDX模型时代已经过去,原因在于CDX模型缺乏肿瘤特异性和肿瘤的生长环境并且与临床病人缺乏相关性。研究表明,CDX模型筛选的药物在二期临床试验中的有效率仅为30%左右。 与使用肿瘤细胞系开发的异种移植模型不同,PDX模型中肿瘤可以从患者身上获得后立即植入,而不需要任何培养。虽然PDX模型成功率相对要低一些,但是PDX模型可以更好地反映出肿瘤的遗传多样性,更加真实地模拟患者的情况,更好地预测肿瘤对于不同药物的反应。
PDX模型跟临床的药效学结果有极高的相关性,因此在新药研发的诸多关键节点(如药物筛选,药效验证,临床试验病人筛选等)得到了越来越广泛的应用。如今,PDX动物模型在癌症研究领域的影响力日益剧增。
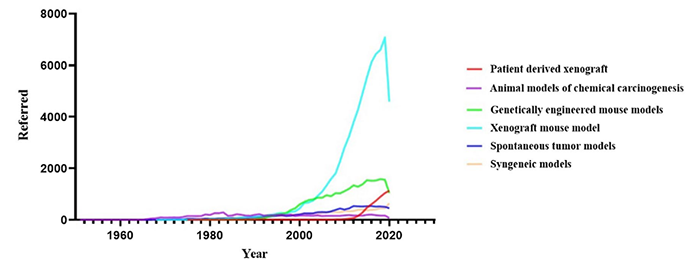
(DOI: 10.1186/s12967-022-03405-8)
二、PDX模型的构建方法
PDX有两种不同的来源材料:一种是单细胞悬液,一种是组织碎片。
将肿瘤患者的新鲜实体瘤组织经过裁剪(去除肿瘤表面连带的组织、肿瘤外膜及肿瘤内钙化坏死部分)后放置于培养液中,处理成大小均匀的小块(或进行化学消化或物理处理成单细胞悬浮液),然后后接种到免疫缺陷的小鼠上,依靠小鼠提供的微环境进行生长,在小鼠身上成瘤以后可以进一步传代。这种模型保留了原代肿瘤的微环境和细胞的基本特性,形成第1代移植瘤。 待其生长到一定大小时取该移植瘤组织无菌操作再移植到新一批鼠体内,形成第2代移植瘤。如此重复操作形成移植瘤第3代、第4代等。 移植瘤传至第2或第3代才能够稳定生长(生长曲线一致性较高,潜伏期趋于稳定)。为了保证与原发肿瘤的一致性,PDX模型传代次数一般不超过10代。 (DOI:10.3390/cells8080889)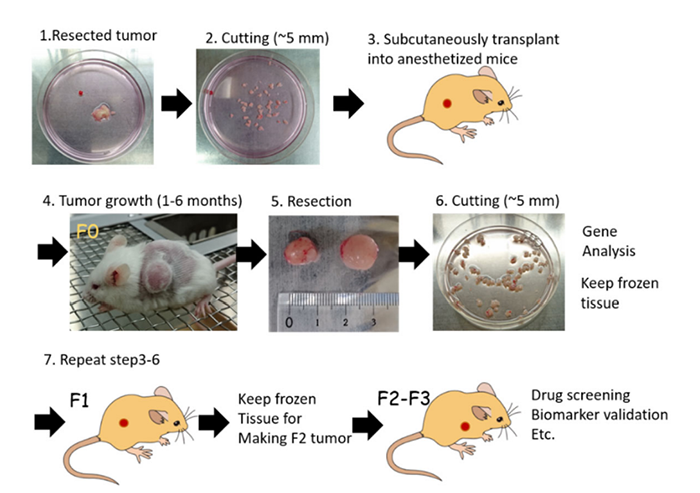
肿瘤碎片保留了原始肿瘤的细胞间相互作用和一些组织结构,因此模拟了肿瘤的微环境。
而单细胞悬液能够收集整个肿瘤的无偏样本,避免在分析或肿瘤传代过程中无意富集某些亚克隆。然而,单细胞悬浮液使肿瘤细胞在受到化学或机械力后,可能会引发细胞凋亡,从而影响细胞活性和植入的成功率。
PDX模型的成瘤时间差异性比较大,主要看肿瘤类型,一般不超过12周。食道癌的成瘤时间最短,一般1个月就可以成瘤,脑癌与乳腺癌的成瘤时间最长,一般需要6个月左右。其它如肺癌,肝癌等常见肿瘤一般在2-4个月就可以成瘤了。
PDX模型的验证和分析
当移植的肿瘤达到足够大小(直径为1-2cm)时,切取肿瘤,应尽可能切除肿瘤周围的小鼠组织。
用10%的福尔马林保存一部分肿瘤,并用苏木精和伊红或其他免疫组织化学标记物进行染色,以验证PDX的组织学与原始肿瘤是否保守。
另一部分可冷冻处理,可进行基因/蛋白质表达定性或定量检测、转录组学、蛋白质组学及代谢组学检测。
推荐阅读:速看,动物实验这些取样细节,你有注意吗?
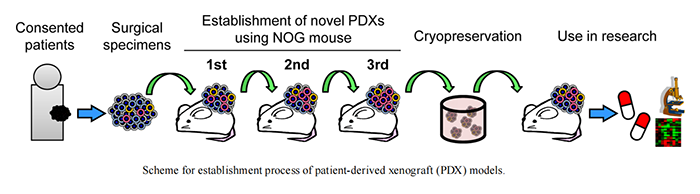
(DOI: 10.1293/tox.2020-0007)
影响PDX模型植入成功率的因素
PDX的成功率还不高,根据文献报道,目前移植成功率在23-75%之间。
PDX的成功率受多种因素的影响。 ①跟肿瘤本身相关。 原发肿瘤的特征,包括肿瘤的侵袭性、组织学类型、肿瘤细胞在组织中所占比例是极其重要的。肿瘤对宿主环境的适应能力因原始肿瘤而异,能很好地适应环境而没有免疫排斥反应的肿瘤组织更有可能植入成功。 ②与操作过程有关。 a.组织应该尽可能新鲜,从手术室到实验室所需的时间应该尽可能短,且手术后的组织需要立即保存在寒冷、新鲜的介质中。 b.植入的组织的大小和数量可能是影响成功率的重要因素。碎片数量越多,成功率越高,碎片大小应为1-2 mm3。 c.植入部位不同,成功率也不同。PDX模型的构建主要有三种方式: 皮下移植:直接种植在小鼠的皮下,一般选择血运淋巴回流丰富的腹股沟和腋窝,是最常用也是最简单的构建方式。 肾被膜移植:对动物操作要求比较高,但是肾被膜下血运较为丰富,所以其成瘤率较高。比较适合那些对肿瘤营养环境要求苛刻的肿瘤细胞。 原位移植:生长环境与原发肿瘤接近,较好的反应肿瘤的生物学特性,但是原位移植的操作难度最高,且小鼠手术后死亡率较高,很少有实验室可以做出原位移植,现阶段比较成熟的原位移植是肠的原位移植。 ③和宿主老鼠相关。 PDX模型是将人的肿瘤组织移植到小鼠体内,并利用小鼠的身体环境来支持肿瘤组织生长的一种动物模型。所以在制备PDX模型的过程中最好选择对异源肿瘤组织排斥率较低的宿主小鼠,也就是免疫缺陷小鼠。免疫缺陷程度越高的小鼠在构建PDX模型时成功率越高! 现阶段在市场上常用的免疫缺陷小鼠有:裸鼠,SCID小鼠,NOD-SCID小鼠以及NSG小鼠。其中NOD-SCID和NSG小鼠,可以大大提高异种移植的效率,是PDX小鼠模型的理想来源。 由于雌激素有一定的免疫保护作用,我们一般选择雄鼠造模,选择上4-6周刚成年的小鼠。此外还要准备胎牛血清包裹肿瘤组织提高成瘤率。
考虑到病人肿瘤样本的珍贵性,PDX模型成瘤率60-70%才是比较可以接受的,但是当前部分癌种还是难以做到这一点的。
三、PDX模型的应用
(1)药物筛选
本世纪初德国科学家率先使用PDX模型进行药物筛选,经过大约20年的验证,大家发现利用PDX模型进行药物筛选的结果跟临床的相关性高达89%~90%,所以全球的药厂现在都逐步采用PDX模型进行肿瘤药物的筛选,目前已有不少利用PDX模型筛选出的抗肿瘤新药走上了临床。
(2)指导用药
PDX模型已成为评估药物疗效和药物敏感性的有力工具,也称为PDX临床试验。
在当前的治疗中,手术以后化疗和靶向药物治疗存在着很多的随机性与盲目性。往往一线药根据指南使用过之后,二三线药的选择具有很大的随机性。
PDX模型小鼠是肿瘤患者的的完美替身,可替代肿瘤患者对不同的治疗药物或方案进行体内药效学检测,更是试药的完美替身,通过将二,三线治疗药物进行排序,从中筛选出最优的治疗药物或方案作为临床用药参考,可以提高肿瘤患者临床治疗的有效性。
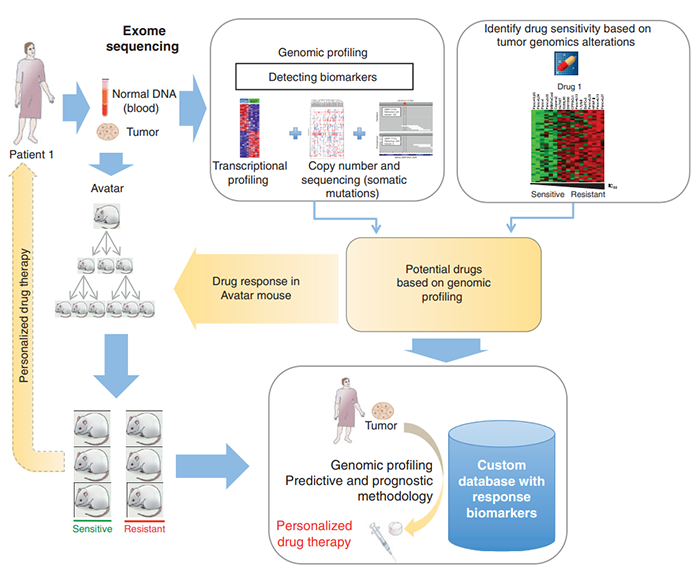
(DOI: 10.1158/2159-8290.CD-14-0001)
(3)探索新靶标
PDX模型还可以被用来寻找新的肿瘤标志物,进行肿瘤克隆演化、肿瘤分子特征、肿瘤致病机制等方面的研究。
(4)探索生物标志物与耐药机制
PDX模型还可以用于进行肿瘤的生物标志物预测,来判断药物敏感或者耐药。结直肠癌的PDX模型结果显示KRAS突变肿瘤对EGFR抗体西妥昔单抗没有反应,KRAS野生型现在是该靶向治疗方案的临床标志物。
结语
PDX模型在辅助临床的作用上有着先天优势,其保留原有肿瘤组织的方式让它的试验结果更接近于人体试验,对肿瘤临床前评估、治疗和预后具有重要的转化意义,有望为肿瘤患者个体化治疗带来新突破。
参考文献
【1】The Generation and Application of Patient-Derived Xenograft Model for Cancer Research,DOI: 10.4143/crt.2017.307
【2】Patient-derived xenograft (PDX) models, applications and challenges in cancer research,DOI: 10.1186/s12967-022-03405-8
【3】Patient-derived xenografts: a relevant preclinical model for drug development,DOI: 10.1186/s13046-016-0462-4
【4】Towards precision oncology with patient-derived xenografts,DOI: 10.1038/s41571-022-00682-6
【5】Patient-derived xenograft (PDX) models: characteristics and points to consider for the process of establishment,DOI: 10.1293/tox.2020-0007
【6】Application of Highly Immunocompromised Mice for the Establishment of Patient-Derived Xenograft (PDX) Models,DOI:10.3390/cells8080889
【7】Patient-derived xenografts effectively capture responses to oncology therapy in a heterogeneous cohort of patients with solid tumors, DOI: 10.1093/annonc/mdx416
【8】Patient-derived xenograft models: an emerging platform for translational cancer research, DOI: 10.1158/2159-8290.CD-14-0001
【9】PDX Models: History and Development,DOI:10.1016/B978-0-12-804010-2.00001-1
【10】Mouse Models for Cancer Immunotherapy Research, DOI: 10.1158/2159-8290.CD-18-0044














