PI3K信号通路是细胞内重要的信号转导通路之一,也是癌细胞中常见的异常表达信号通路。PI3K信号通路参与了细胞增殖、分化、凋亡和葡萄糖转运等多种细胞功能的调节,PI3K、Akt和mTOR是该通路的3个重要“连接点”,其中PI3K通过将PIP2转化为PIP3激活下游效应因子,在该通路中扮演着关键角色1-3(图1)。
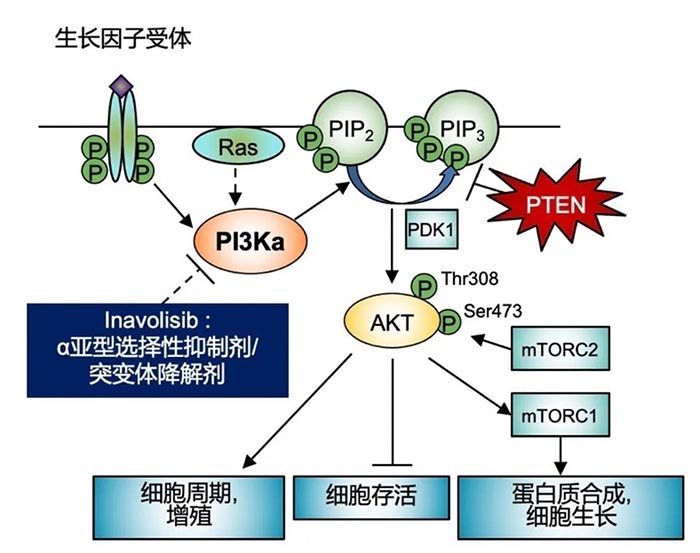
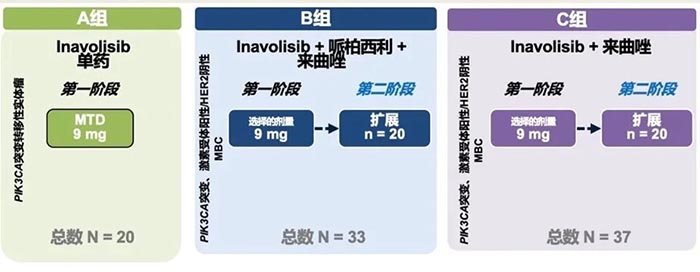
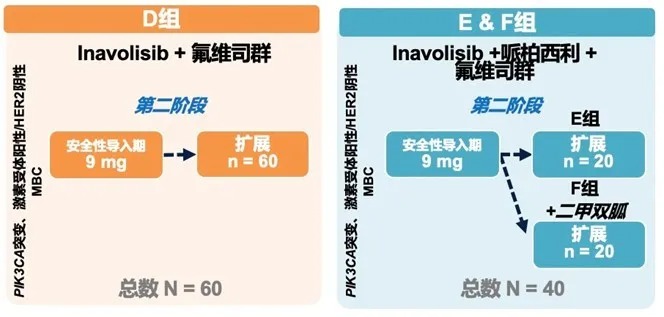
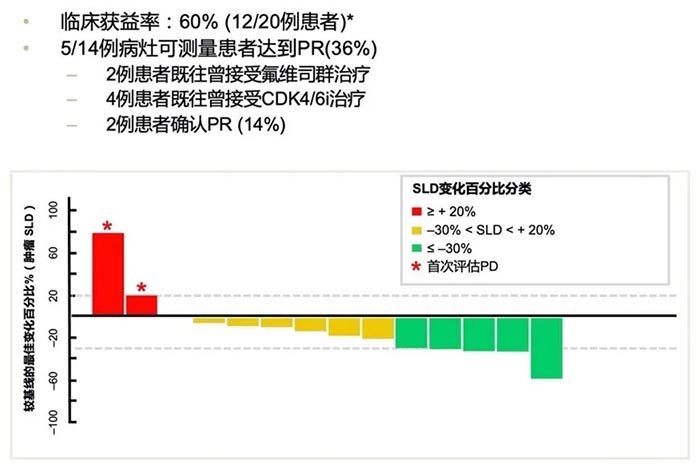
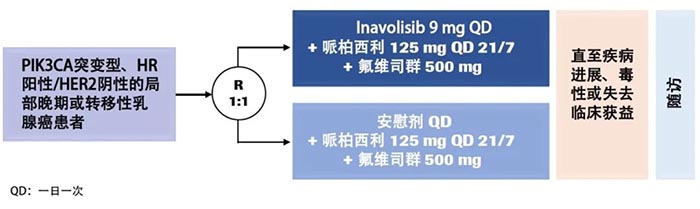
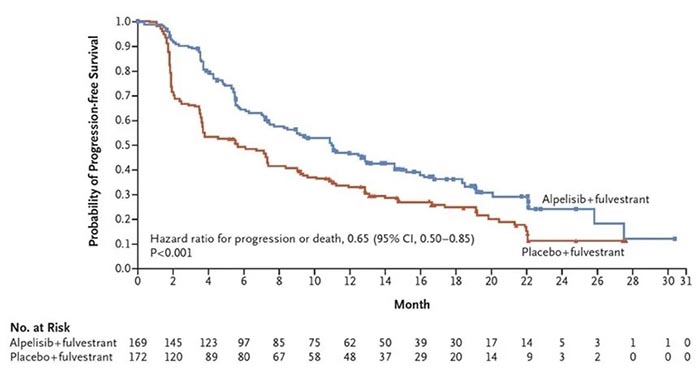
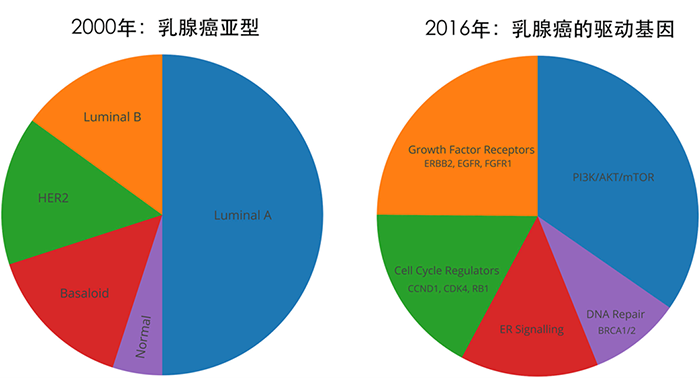
图1 PI3K/Akt/mTOR信号通路是调节蛋白质合成的主要信号通路,促进细胞周期进展,细胞生存、增殖和分化。 注:AKT,蛋白激酶B;mTORC1,哺乳动物雷帕霉素靶蛋白复合物 1;mTORC2,哺乳动物雷帕霉素靶蛋白复合物 2;PDK1,磷酸肌醇依赖性激酶-1;PI3K,磷脂酰肌醇 3-激酶;PIK3CA,磷脂酰肌醇-4,5-二磷酸 3-激酶,催化亚基 α;PIP2,磷脂酰肌醇-3,4-二磷酸;PIP3,磷脂酰肌醇-3,4,5-三磷酸;PTEN,磷酸酶和张力蛋白同源物;RTK,受体酪氨酸激酶 PI3Ks是一种脂质激酶蛋白家族,分为三类(I,II和III),各亚型的结构与功能各异,目前研究最广泛的为I类PI3K。I类PI3Ks可细分为IA和IB两个亚型,由一个调节亚基(p85)和一个催化亚基(p110)组成,其中催化亚基p110有四种亚型结构,所以I类PI3Ks又可分为PI3Kα、PI3Kβ、PI3Kδ以及PI3Kγ。PI3Kα分布于各组织器官,与癌症密切相关4。 乳腺癌的发生与PI3K信号通路的异常激活及其相关基因突变有关,最常见的突变基因为PIK3CA(组成PI3Kα的p110α由该基因编码)。研究发现,约40%的HR阳性/HER2阴性乳腺癌患者会发生PIK3CA基因突变5。 此外, PI3K信号通路转导异常与乳腺癌内分泌治疗耐药密切相关,内分泌耐药模型中可见PI3K通路常过度活化6。总之,针对PI3K信号通路的靶向治疗可抑制肿瘤细胞的生长增殖,促使其凋亡,且联合内分泌治疗可产生协同效果。 医脉通:日前,中国国家药监局药品审评中心(CDE)公布,在研新药PI3Kα抑制剂Inavolisib(GDC-0077)已在中国获批临床试验。您能否介绍一下这一抗癌新药及其作用机制? 宋传贵教授:Inavolisib是一种PI3Kα特异性抑制剂和突变体降解剂,相较于其他PI3Ks,其对PI3Kα的选择性更强(Inavolisib对PI3Kα的选择性是对其他I类PI3K亚型的300倍)。此外,Inavolisib可以蛋白酶体依赖性方式诱导p110α突变体降解,使PI3K异常表达信号通路无法被激活,从而更强力、更持久地抑制肿瘤细胞增殖和生长(图2)。在PIK3CA突变型乳腺癌移植瘤模型中,Inavolisib单药及与抗雌激素联合治疗均显示出抗肿瘤活性7。 图2 inavolisib的作用机制 注:AKT,蛋白激酶B;mTORC1,哺乳动物雷帕霉素靶蛋白复合物1;mTORC2,哺乳动物雷帕霉素靶蛋白复合物 2;PDK1,磷酸肌醇依赖性激酶-1;PI3K,磷脂酰肌醇 3-激酶;PIK3CA,磷脂酰肌醇-4,5-二磷酸 3-激酶,催化亚基 α;PIP2,磷脂酰肌醇-3,4-二磷酸;PIP3,磷脂酰肌醇-3,4,5-三磷酸;PTEN,磷酸酶和张力蛋白同源物;RTK,受体酪氨酸激酶;Ser473,丝氨酸 473;Thr308,苏氨酸 308 目前有两项Inavolisib临床研究正在开展。一项为开放标签、剂量递增的I/Ib期研究,评估在PIK3CA突变、HR阳性/HER2阴性转移性乳腺癌患者中,Inavolisib单药和联合内分泌治疗+CDK 4/6抑制剂哌柏西利的疗效和安全性(图3)。结果提示,Inavolisib单药及联合治疗均显示出抗肿瘤活性,以及可控的安全性8-10。 图3 一项在PIK3CA突变、HR阳性/HER2阴性转移性乳腺癌患者中评价Inavolisib单药和联合内分泌治疗 + 哌柏西利的 I/Ib 期研究(NCT03006172) 在A组中,Inavolisib单药治疗显示出初步抗肿瘤活性和可控的安全性,20例患者中有5例观察到部分缓解,最佳总体缓解率(best overall response,BOR)达25%,临床获益率(clinical benefit rate,CBR)达45%,并确定最大耐受剂量为9mg8。在B组中,Inavolisib+标准来曲唑+哌柏西利同样表现出良好的初步抗肿瘤活性,有15例患者观察到部分缓解(BOR率:46%),CBR达79%。C组中,Inavolisib+来曲唑治疗后,6例患者观察到部分缓解(BOR率:16%)9。 D组中,Inavolisib联合氟维司群显示出可控的安全性,与Inavolisib单药相似的药代动力学,初步的抗肿瘤活性,以及对ctDNA中PIK3CA突变等位基因频率具有药效学(Pharmacodynamics,PD)调节作用(图4)。同时提示,进食不影响Inavolisib单次给药后或稳态时的吸收速率或程度10。 图4 D组研究的初步结果分析 注:*临床获益率:SD≥24 周、PR或CR;C,周期;CDK4/6i,细胞周期蛋白依赖性激酶 4/6 抑制剂;CR,完全缓解;ctDNA,循环肿瘤DNA;D,天;MAF,突变等位基因频率;PD,疾病进展;PR,部分缓解;SD,疾病稳定;SLD,最长径总和 另一项名为INAVO120的随机双盲、安慰剂对照的的全球III期研究目前正在进行中,评价Inavolisib+哌柏西利+氟维司群联合应用在PIK3CA突变型、HR阳性/HER2阴性的局部晚期或转移性乳腺癌患者的疗效和安全性(图5)11。该研究目前正在入组阶段,预计将在全球210个中心入组约400例患者。研究的主要终点为PFS,次要终点包括ORR、BOR、DOR和OS等。目前福建医科大学附属协和医院也将参与这项研究,欢迎符合条件的患者来我中心咨询。 图5 INAVO120研究设计 目前在研的PI3Kα抑制剂都有哪些?进展如何? 除了Inavolisib外,目前在研PI3Kα抑制剂包括alpelisib、taselisib、MLN-1117和ASN003(PI3Kα和BRAF V600E/K双重抑制剂)。这些药物均已进入临床研究阶段,在PIK3CA突变、耐受性良好的患者中显示出良好的疗效。与广谱型PI3K抑制剂相比,PI3Kα特异性抑制剂脱靶效应更小12。 Alpelisib的III期研究结果显示,对于在内分泌治疗期间或之后疾病进展的PIK3CA突变、HR阳性/HER2阴性晚期乳腺癌患者,与接受安慰剂+氟维司群治疗相比,接受alpelisib+氟维司群治疗患者的PFS显著较长(11.0 vs. 5.7个月;P<0.001),且估计疾病进展或死亡风险降低35%13(图6)。2020年欧洲肿瘤内科学会(ESMO)年会公布了SOLAR-1研究的最终OS分析结果,在PIK3CA突变队列中, Alpelisib+氟维司群治疗较安慰剂+氟维司群组的中位OS延长了7.9个月(39.3 vs. 31.4个月),但并未达到统计学差异(HR:0.86;P=0.15)。进一步亚组分析显示,对于有肺/肝脏转移的患者,接受Alpelisib+氟维司群治疗较安慰剂+氟维司群治疗中位OS延长了14.4个月(37.2 vs. 22.8个月;HR:0.68);而对于血浆ctDNA中检测出PIK3CA突变的患者,接受Alpelisib+氟维司群治疗较安慰剂+氟维司群组的中位OS延长了9.2个月(34.4 vs. 25.2个月;HR:0.74)14。该研究表明,在PIK3CA突变、HR阳性/HER2阴性晚期乳腺癌的标准治疗加用PI3Kα抑制剂可改善患者结局,证实PIK3CA是该患者人群的一个重要治疗靶点。 图6 Kaplan-Meier分析:在PIK3CA突变癌症患者队列中,alpelisib+氟维司群组 vs. 安慰剂+氟维司群组的PFS13 taselisib的首个临床研究入组了34位晚期实体瘤患者患者,在接受taselisib治疗后,有PIK3CA突变患者队列的ORR为36%(5/14),而没有PIK3CA突变患者队列的ORR为0%(0/15)15。 据悉,美国FDA已批准FoundationOne CDx用作alpelisib联合氟维司群的伴随诊断16。您能否为我们讲解一下该技术是如何指导PI3Kα抑制剂更精准地治疗乳腺癌患者的? 如上所述,PI3Kα抑制剂单药或联合治疗可使有PIK3CA突变的癌症患者显著获益,而如何寻找到有PIK3CA突变的患者是这一治疗方案得以实施的关键。FoundationOne CDx是一种二代测序(NGS)技术,其原理是将分离的单个细胞的微量全基因组DNA进行扩增,获得高覆盖率的完整的基因组后进行高通量测序。该技术可检测乳腺癌中的多个PIK3CA突变位点,指导PI3Kα抑制剂的精准治疗17。 有研究为8 654例晚期乳腺癌患者使用NGS技术诊断,结果在6 959例患者中发现至少一种基因突变,超过半数的乳腺癌患者(51%)存在PI3K通路异常且对靶向该通路的抑制剂敏感18。可以看到,通过NGS检测可将乳腺癌基于驱动基因分类(图7),更精确地指导靶向药物的治疗。 图7 基于亚型(左)或驱动基因(右)的转移性乳腺癌分类18 SOLAR-1研究中的PIK3CA突变通过PCR方法进行,后使用FoundationOne CDx对71%的样品进行回顾性测序,在PCR检测PIK3CA突变阴性的患者中有16%通过FoundationOne CDx检测到了PIK3CA突变,而在PCR检测PIK3CA突变阳性的患者中有93%通过FoundationOne CDx检测到PIK3CA突变。总体而言,通过PCR评估的PIK3CA突变患者队列中,接受alpelisib+氟维司群治疗患者的疾病进展风险降低了35%;而通过FoundationOne CDx评估的PIK3CA突变患者队列中,患者的疾病进展风险降低了45%13,19。 结语 许多乳腺癌患者存在PI3K基因突变,导致PI3K蛋白通路异常活化,其多数的突变位点位于PIK3CA基因。随着抗癌领域精准诊疗时代的来临,以PI3K蛋白信号通路中的关键分子为靶点的抗癌治疗已成为研究热点。作为强选择性PI3Kα抑制剂,Inavolisib(GDC-0077)已在PIK3CA突变、HR阳性/HER2阴性乳腺癌患者中显示出良好的抗肿瘤活性,和可控的安全性。此外,备受瞩目的III期INAVO120研究目前正在入组阶段,福建医科大学附属协和医院将作为其中一家中心开展该研究,该研究旨在进一步评价Inavolisib+哌柏西利+氟维司群联合应用在PIK3CA突变型、HR阳性/HER2阴性的局部晚期或转移性乳腺癌患者的疗效和安全性。总之,在乳腺癌领域,PI3Kα抑制剂已取得突破性进展,值得持续关注。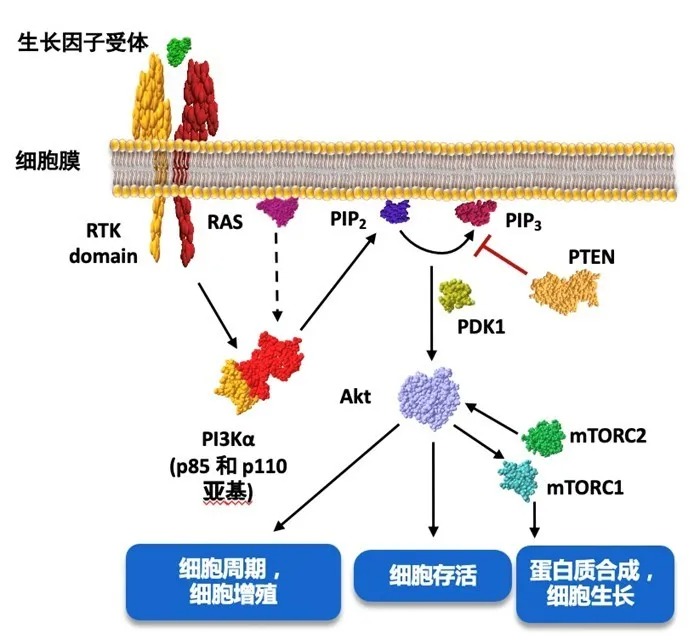
参考文献:
1. Ma CX, Ellis MJ. The Cancer Genome Atlas: clinical applications for breast cancer. Oncology (Williston Park). 2013 Dec;27(12):1263-9, 1274-9.
2. Engelman JA. Targeting PI3K signalling in cancer: opportunities, challenges and limitations. Nat Rev Cancer. 2009 Aug;9(8):550-62. doi: 10.1038/nrc2664.
3. Paplomata E, O'Regan R. The PI3K/AKT/mTOR pathway in breast cancer: targets, trials and biomarkers. Ther Adv Med Oncol. 2014 Jul;6(4):154-66. doi: 10.1177/1758834014530023.
4. Foster JG, Blunt MD, Carter E, et al. Inhibition of PI3K signaling spurs new therapeutic opportunities in inflammatory/autoimmune diseases and hematological malignancies. Pharmacol Rev. 2012 Oct;64(4):1027-54. doi: 10.1124/pr.110.004051.
5. Vasan N, Toska E, Scaltriti M. Overview of the relevance of PI3K pathway in HR-positive breast cancer. Ann Oncol. 2019 Dec;30 Suppl 10:x3-x11. doi: 10.1093/annonc/mdz281.














