由于ceRNA机制研究的套路较为固定,调控网络的预测相对简单,实验也并不复杂,因此近年来非编码RNA的研究大多从ceRNA机制研究这一角度着手,相关文章数量出现井喷式增长,这势必导致ceRNA机制研究落入俗套,出现ceRNA研究难发高分文章的现象。今天胖师兄给大家分享两篇文章,ceRNA研究套路一样,都是生信数据挖掘+实验验证,一篇发表在Molecular Cancer上,影响因子10.68,一篇发表在OncoTargets and Therapy上,影响因子3.05,通过这两篇文章我们来谈谈如何在ceRNA机制研究套路上玩出新花样。
既然是做ceRNA机制研究,那么首先要确定的是作为ceRNA的非编码RNA,比如lncRNA,然后在确定lncRNA之后顺藤摸瓜找到lncRNA sponge的miRNA以及靶向miRNA的mRNA,最终确定lncRNA-miRNA-mRNA这一ceRNA调控网络,当然这中间的各种验证实验是必不可少的。
我们按照这样的ceRNA研究思路先来看下第一篇文章是如何阐述乳腺癌中ceRNA调控网络的。

1) 确定目标lncRNA
首先研究人员分析了公共数据库TCGA和GEO(GSE112848)中乳腺癌相关的lncRNA,确定研究目标BCRT1。然后对该lncRNA的结构和编码能力进行了分析,并分析了细胞和组织中该lncRNA的表达情况,以及该lncRNA表达量与临床预后的相关性,结果均显示该lncRNA与乳腺癌密切相关,最后进行了亚细胞定位,以便后续从ceRNA的角度进行分析。
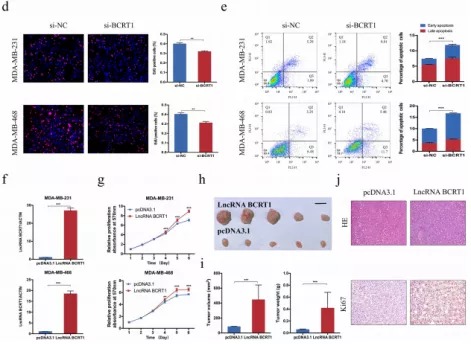
体内外沉默/过表达BCRT1,观察细胞表型变化和小鼠肿瘤的变化,结果显示BCRT1促进乳腺癌细胞的增殖、迁移、侵袭,减缓细胞凋亡,加速小鼠肿瘤组织的增长和血管生成,促进癌转移,提示BCRT1影响乳腺癌进展。
(从众多的差异lncRNA中挑出有研究价值的lncRNA并不容易,锁定目标lncRNA后一定要进行充分分析,体内外功能实验+临床分析,确保目标lncRNA与乳腺癌密切相关)
2) 确定miRNA
确定目标lncRNA后,分析靶向lncRNA的miRNA。通过RegRNA数据库预测靶向miRNA miR-1303,荧光素酶及RIP实验证实了两者的结合关系。体内外沉默/过表达BCRT1,结果显示BCRT1和miR-1303表达负相关。
临床分析显示miR-1303对应良好预后,功能实验表明miR-130抑制细胞增殖、迁移和侵袭,促进凋亡能力,而功能挽救实验进一步说明BCRT1与miR-1303之间存在拮抗作用。
(lncRNA靶向的miRNA不少,如何选择其中的一个miRNA进行后续分析,作者没有详细说明,想必中间也有不少的工作量。靶向miRNA除了要与目标lncRNA密切相关外,还要与乳腺癌密切相关,这里的功能实验和临床分析同样有必要做下)。
3) 确定mRNA及三者关系
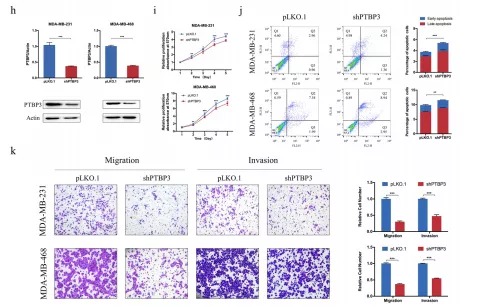
确定了lncRNA和miRNA,就需要确定最后的mRNA了。利用miRDB、miRWalk、miRPathDB和TargetScan预测miR-1303的靶基因,确定PTBP3。利用TCGA和GEO数据分析PTBP3在乳腺癌中的表达水平,并对PTBP3的临床预后,与BCRT1结合关系以及表达相关性进行了分析。利用沉默/过表达以及回复实验确定了BCRT1、miR-1303和PTBP3三者之间表达相关性,并通过细胞功能实验表明PTBP3促进乳腺癌细胞增长。
(找到miRNA的靶mRNA后,将lncRNA-miRNA-mRNA三者联系起来,并且准确说明这一ceRNA网络确实影响癌症的发生发展,至此一个较为完整的ceRNA调控网络就基本形成了。)
4) 外泌体+巨噬细胞极化
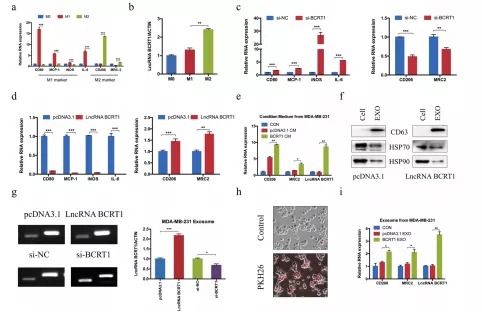
完成上述ceRNA调控网络分析后,研究人员进行了扩展研究,将BCRT1与巨噬细胞的M2极化进行了关联分析。沉默/过表达BCRT1提示其能影响巨噬细胞M2极化。进一步研究发现BCRT1可能通过外泌体途径影响M2极化,共培养等实验表明外泌体BCRT1可以进入巨噬细胞,促进M2极化,并促进细胞迁移和血管生成。
(研究人员不仅从ceRNA角度阐述了BCRT1与乳腺癌的关系,还引入常见的癌症研究方向即巨噬细胞的M2极化,另外还加入了外泌体这一研究热点,为文章增色不少。)
5) 低氧+转录因子
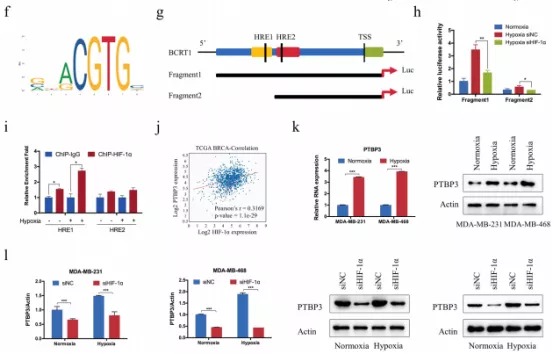
低氧是肿瘤微环境的主要特征之一,在证明BCRT1与巨噬细胞的M2极化有关后,研究人员分析了BCRT1与低氧的关系,结果显示低氧处理上调BCRT1和HIF-1α的表达。利用JASPAR数据库以及荧光素酶和ChIP实验分析发现转录因子HIF-1α能结合到BCRT1启动子上,调控其表达。
进一步分析发现低氧能提高PTBP3的表达,增强细胞增殖能力。敲减HIF-1α或BCRT1能缓解低氧引起的作用,而过表达BCRT1则可部分逆转HIF-1α敲减引起的抑制作用。此外,研究发现BCRT1参与低氧引起的EMT过程。
(继ceRNA调控网络,巨噬细胞M2极化后,作者又引入低氧这一研究方向,从多层面多角度阐述了BCRT1这一lncRNA与乳腺癌发生发展的关系。)
第二篇文章是关于肝细胞癌(HCC)的,该文同样是生信分析+实验验证,文章的整体思路与上文ceRNA网络研究部分一致,但影响因子却低很多,除了没有进行扩展分析外,ceRNA研究这一部分生信分析和实验验证都相对薄弱。
1) 确定目标lnRNA
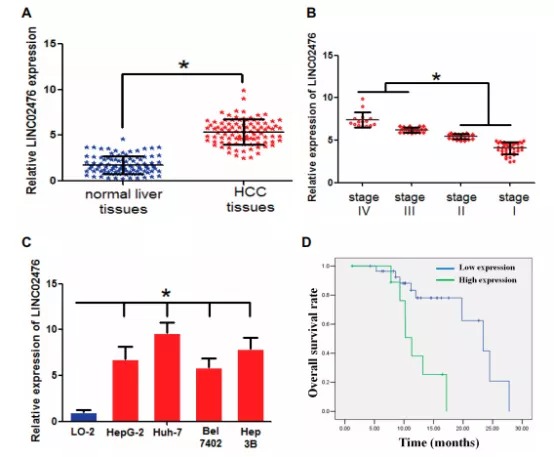
研究人员首先分析了TCGA中HCC相关的lncRNA,确定目标LINC02476。对HCC细胞及患者中的LINC02476水平进行了检测,并对其编码能力和亚细胞定位进行了分析。临床分析显示LINC02476与肿瘤大小、淋巴结转移及疾病分期相关,并预示良好预后。功能实验表明敲减LINC02476,细胞增殖、侵袭能力下降,细胞大多停留在G1期。
(lncRNA与HCC的关联分析稍显薄弱,功能实验只做了体外的敲减,没有做过表达,另外也没有做体内实验。)
2) 确定miRNA
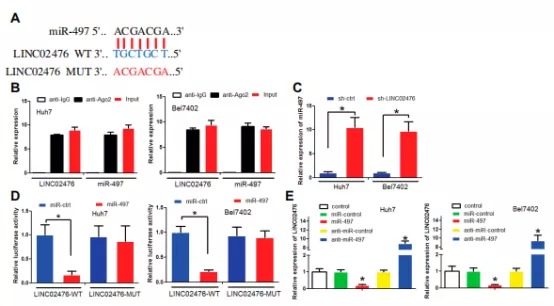
确定目标lncRNA后,研究人员利用miRDB预测了靶向结合的miRNA,并挑选有报道的miR-497进行后续分析。荧光素酶结合RIP实验证明了LINC02476与miR-497的结合关系。敲减LINC02476,miR-497的表达升高,而沉默/过表达miR-497,LINC02476的表达升高/降低。
(靶向miRNA的确定缺乏严谨性,miR-497与HCC生物学功能,临床相关性,在细胞和组织中的表达量均没有研究说明。)
3) 确定mRNA及三者关系
利用TargetScan预测到miR-497靶基因HMGA2。荧光素酶报告实验证实miR-497与HMGA2的结合,沉默/过表达及挽救实验证实LINC02476、miR-497和HMGA2三者之间存在的表达关系符合ceRNA调控理论。体外实验表明沉默LINC02476引起的细胞生长、侵袭和周期分布等变化在过表达HMGA2后消失,体内实验表明沉默LINC02476,肿瘤大小体积及生长速度明显下降,HMGA2表达量降低。
(这一步没有在HCC细胞和组织中分析HMGA2表达量,也未对HMGA2与HCC展开功能和临床分析,另外,LINC02476,miR-497,HMGA2三者之间关系验证的实验也较为单薄。)
两篇文章都进行了lncRNA的ceRNA机制研究,相对来说第一篇文章的研究内容更为丰富,除了ceRNA研究外,扩展研究部分为文章增色不少。但单看两篇文章的ceRNA机制研究,不难看出第一篇文章不管是数据挖掘还是验证实验都更为丰富和严谨,即使没有扩展研究,单纯的ceRNA研究也比第二篇优秀不少。所以说套路还是那个套路,但一定要严谨,该做的分析一定要做全,牢牢套住套路。














