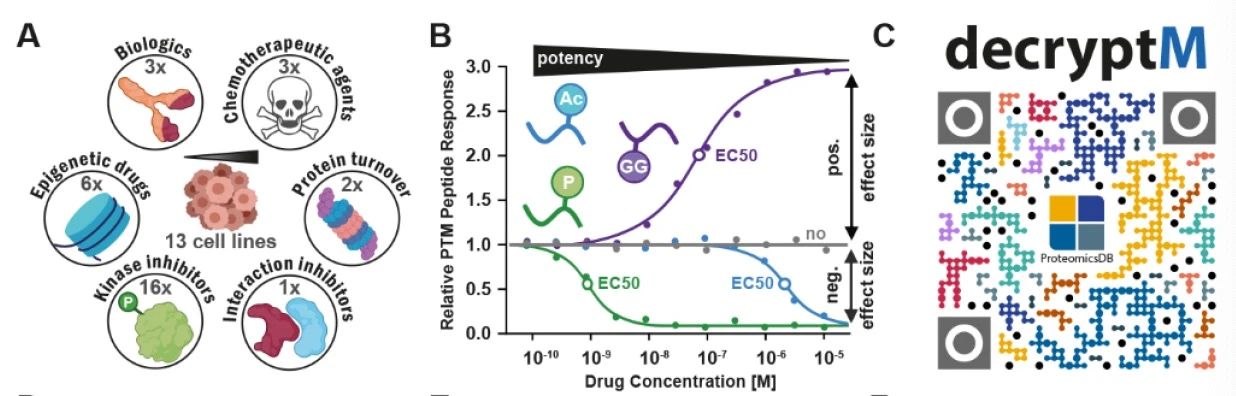
大部分作用于蛋白质的药物,它们本身是蛋白质;这些药物蛋白要么通过改变靶标蛋白水平(生产或降解),要么利用细胞的蛋白机制,来发挥它们的疗效作用。药物调节的蛋白质翻译后修饰(post-translational modifications, PMTs)既能够组成分子靶标衔接标记,亦能够鉴定药物调节通路,还能够解释细胞的下游表型应答。PTM特异性抗体最常用于此目的【1-2】。然而,对于药物处理后细胞内的蛋白及蛋白翻译后修饰水平变化情况,即便少数的药物有提供信息,也仅仅只是提供半定量的信息;使得从蛋白质及通路层面对药物作用机制的研究出现偏差。因期待与非期待的多向药理学很常见,也因药物在不同细胞类型之间的响应通常具有差异;因此在蛋白质组尺度去了解药物作用机制变得非常重要。可是,在PTM水平关于药物作用机制的系统性信息几乎没有;更令人吃惊的是,目前缺乏关于药物以剂量-时间依赖方式,在蛋白质及蛋白质翻译后修饰水平对药物效力进行评估的文献【3】。近日,来自德国慕尼黑工业大学、生命科学学院、分子生命科学系, Bernhard Kuster团队,在Science杂志上,在线发表了题为Decrypting drug actions and protein modifications by dose- and time-resolved proteomics的文章,报道了一种名为DecryptM的蛋白质组学测试方法;利用该方法可以系统性地对药物,尤其是癌症治疗药物,以剂量及时间依赖的方式,在不同细胞类型,不同药理方式的基础上,对于蛋白质及蛋白质翻译后修饰水平进行深度剖析。为了对药物效力,以及药物处理后对细胞造成的广泛而深远的影响,尤其是对蛋白质与蛋白质翻译后修饰的影响;研究人员推出了名为DecryptM的方法。DecryptM是一种定量蛋白质组学分析方法,该方法以剂量-时间依赖的方式,对癌症药物处理后细胞内蛋白质翻译后修饰的调节水平进行系统性的定量测试;因此既能测试靶标与通路之间的密切关系,也能评估药物的作用机制。具体操作简化流程为:先用逐渐升高浓度的药物对细胞进行处理-多路用稳定的同位素(tandem mass tags, TMT;除了泛素化)-典型多肽类用色谱分析进行分馏-富集含PTMs的多肽-液相串联质谱(LC-MS/MS)。通过采用上述方法,最终研究人员从人体13种癌细胞的试验中,收集了6大类癌症治疗药物中的31种药物的大数据;如下图所示。图注:A 不同生物学功能药物种类,及13种人癌细胞;B, 180万个蛋白质及PTMs药物剂量响应曲线;C, ProteomicsDB数据平台上本文大数据分享二维码。化疗药物:在慢性骨髓白血病细胞系K562中,分别对紫杉醇、阿糖胞苷和甲氨蝶呤三种药物进行了测试。细胞经30分钟处理后;只有2个多肽响应甲氨蝶呤;紫杉醇处理后,测试的7438个多肽中有7个上调;阿糖胞苷处理使23个磷酸化多肽被调节。蛋白质互作抑制剂:在食管鳞状癌细胞系KYSE-520中,仅对非受体酪氨酸磷酸酶SHP-2 (PTPN11) 的变构抑制剂SHP099进行测试。经30分钟处理后,约有30多个与转录有关的蛋白质表达出现差异。蛋白酶抑制剂:在多发性骨髓瘤细胞系RPMI 822中,测试了硼替佐米和卡非佐米。经多个时间点处理后,大幅度地增加了磷酸化位点的同时磷酸化水平也极大改变。表观遗传药物:在HeLa细胞中,分别对姜黄色素,伏立诺他,A-485,A-486,CUDC-101,MLLT1进行测试。CUDC-101处理使1133个测试的乙酰化多肽中的139上调;A-485下调59个;其余药物数据正文未展示具体数目。激酶抑制剂:在肺癌细胞系A549中,首先对10种激酶抑制剂进行了测试。Pan-激酶抑制剂,十字孢碱 (staurosporine) ,调节了2500多个磷酸化多肽;其余药物调节数目为10~100个左右。接下来,本文研究人员在三种不同的乳腺癌细胞系中,对其余激酶抑制剂进行了测试。抗体:在上述激酶抑制剂测试的三种乳腺癌细胞(SK-BR-3, BT-474, MDA-MB-175)中,对曲妥单抗与帕妥珠单抗进行测试。曲妥单抗几乎没有效果;帕妥珠单抗处理后磷酸化多肽约30个在SK-BR-3中被调节,约150个在BT-474中被调节,约150个在MDA-MB-175中被调节。随后,研究人员在利妥昔单抗敏感细胞系B细胞淋巴瘤细胞系SU-DHL-4及Burkitt's淋巴瘤细胞系Ramos,与利妥昔单抗不敏感细胞系血浆白血病细胞系ARH-77中,分别对利妥昔单抗进行测试(数据参与原文)。综上所述,本文的研究工作具有前瞻性;首次以定量的方式对药物处理后细胞内的蛋白质及蛋白质翻译后修饰水平进行了测试。测试的药物种类繁多;涉及的生物学治疗途径广泛;在单一的生物学治疗途径对多种药物进行测试,尤其是抗体治疗途径;同时也对个别单一药物在不同类型的细胞中进行测试;工作非常细致。本文的研究工作同时也具备系统性其大量的测试了各种药物,在各种细胞中的效力,并收集到约180万个与剂量-时间相关的数据;无疑为优化临床治疗提供了极高参考价值的数据。原文链接:
http://doi.org/10.1126/science.ade3925
1. S. Klaeger, S. Heinzlmeir, M. Wilhelm, H. Polzer, K. Spiekermann, B. Kuster, et al. Kuster, The target landscape of clinical kinase drugs. Science 358, eaan4368 (2017).2 J. R. Lill, W. R. Mathews, C. M. Rose, M. Schirle, Proteomics in the pharmaceutical and biotechnology industry: A look to the next decade. Expert Rev. Proteomics 18, 503–526 (2021).3 H. G. Budayeva, A. Sengupta-Ghosh, L. Phu, J. G. Moffat, G. Ayalon, D. S. Kirkpatrick, Phosphoproteome Profiling of the Receptor Tyrosine Kinase MuSK Identifies Tyrosine Phosphorylation of Rab GTPases. Mol. Cell. Proteomics 21, 100221 (2022).