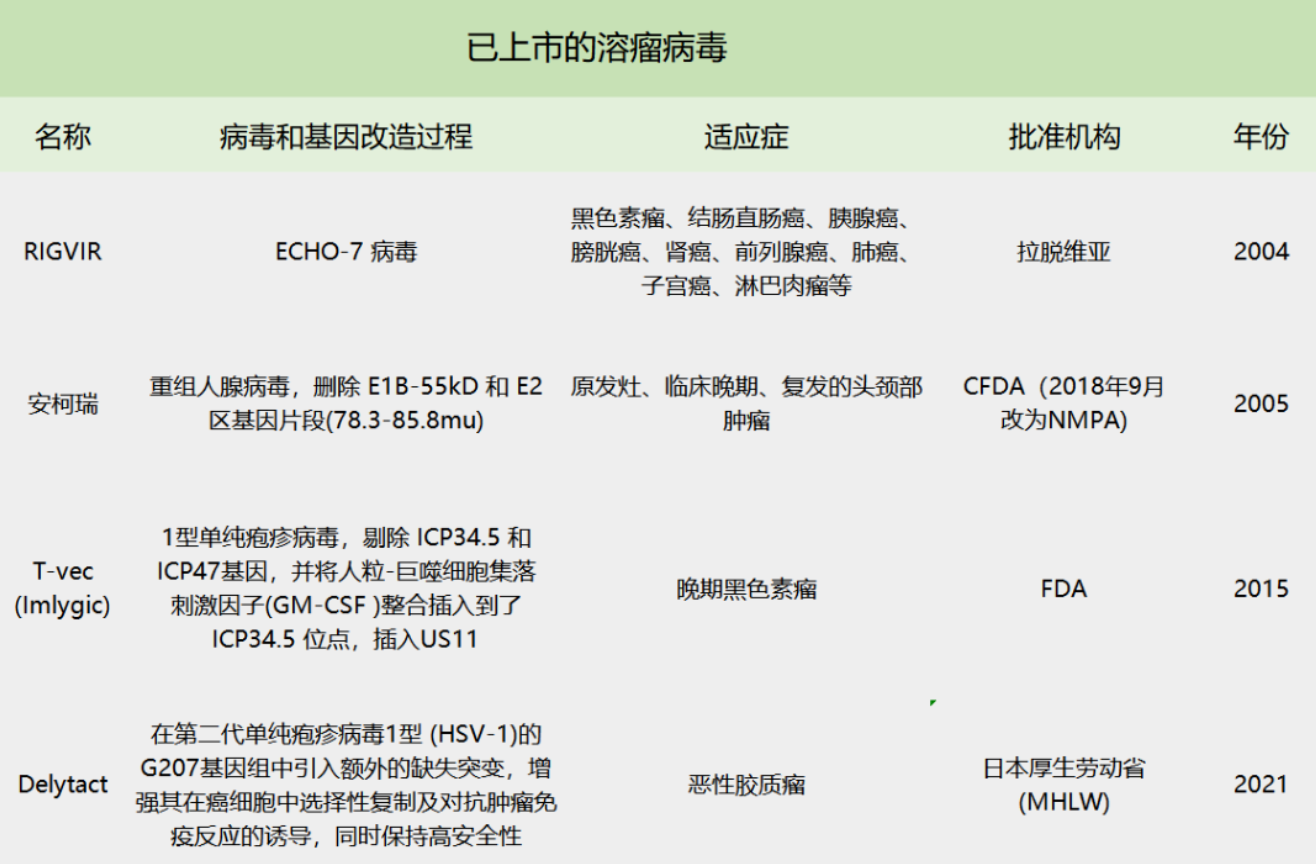
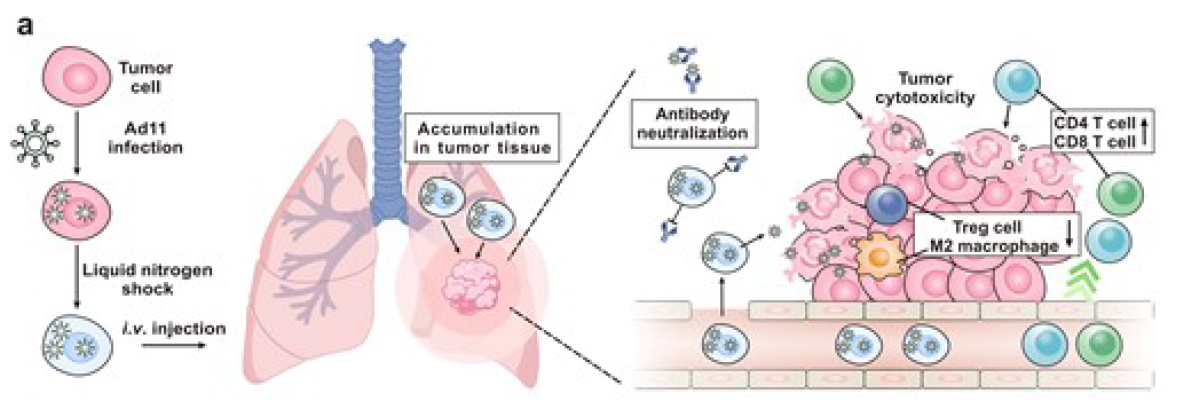
溶瘤病毒(Oncolytic Viruses,OVs)是一种有前途的实体瘤治疗方法。注射到肿瘤内后,溶瘤病毒能够选择性以癌细胞为目标,而不影响正常细胞,通过在癌细胞内复制,导致癌细胞裂解;还能进一步引发全身免疫反应杀伤癌细胞。溶瘤病毒疗法已成为一种有前途的癌症治疗方式。目前,已有4款溶瘤病毒疗法获批通过肿瘤内注射治疗黑色素瘤、结直肠癌、恶性胶质瘤等多种癌症。然而,这种瘤内注射的局部给药途径限制了溶瘤病毒疗法的广泛应用。全身给药的溶瘤病毒可以更容易地到达广泛的肿瘤病灶,但存在巨大的挑战。暴露在血液中的溶瘤病毒颗粒会迅速被补体蛋白灭活,被抗体中和,并被网状内皮系统消除。全身给药后,天然溶瘤腺病毒的半衰期小于2分钟,使得病毒很少到达靶标部位。近日,浙江大学药学院顾臻教授团队在 Advanced Materials 期刊发表了题为:Inhibition of Tumor Metastasis by Liquid Nitrogen-Shocked Tumor Cells with Oncolytic Viruses Infection 的研究论文。该研究描述了一种病毒隐藏的肿瘤靶向策略,使溶瘤病毒可以通过全身给药递送到肺转移肿瘤中。溶瘤病毒可主动感染、内化、隐身于肿瘤细胞内,随后对肿瘤细胞进行液氮冲击处理,消除其致病性。这种类似特洛伊木马的载体避免了溶瘤病毒在血液中的中和和清除,并促进肿瘤靶向递送,使肿瘤转移灶中的病毒富集超过110倍。这一策略可以作为新型肿瘤疫苗,通过增加T细胞的记忆亚型和调节肿瘤免疫微环境,启动内源适应性抗肿瘤作用,包括减少M2巨噬细胞,下调Treg细胞,增强T细胞启动。尽管溶瘤病毒(OVs)具有肿瘤选择性溶解作用,但其系统性给药仍面临循环周期有限、肿瘤靶向性差和自发抗病毒免疫反应等挑战。该研究报道了一种特洛伊木马式的溶瘤病毒给药方法,该方法可在静脉给药后有效靶向递送溶瘤腺病毒11型(Ad11)到肿瘤转移并有效抑制肿瘤发展。
在古希腊神话中,希腊联军围困特洛伊城,却久攻不下,于是假装撤退,并留下一具巨大的木马,特洛伊守军把木马运进城中作为战利品。木马中躲藏的希腊士兵打开城门,导致特洛伊沦陷。后人常用“特洛伊木马”(Trojan Horse)来比喻在敌方埋下伏兵里应外合的活动。
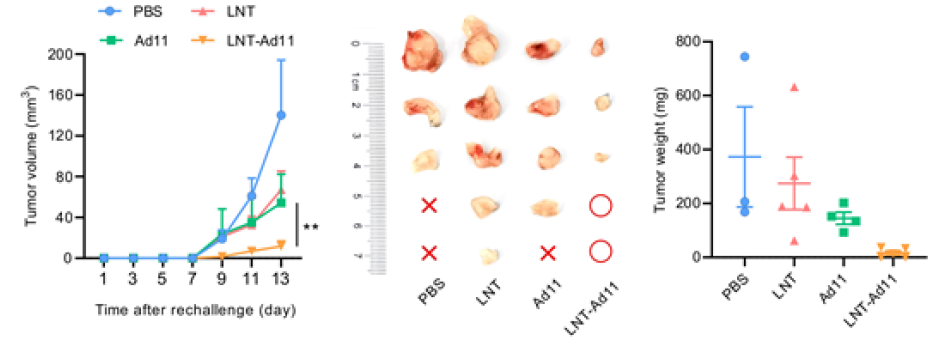
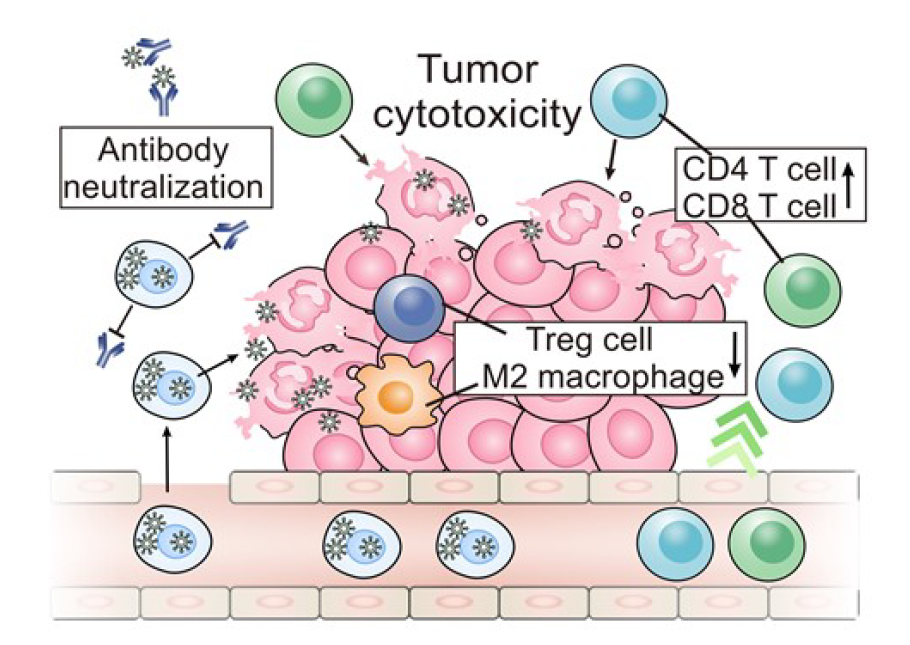
溶瘤病毒可通过CD46介导的内吞作用内化到肿瘤细胞中。在不牺牲溶瘤病毒活性和感染性的情况下,采用液氮冲击消除了肿瘤细胞的致病性。当通过静脉注射后暴露于血液中时,经过液氮冲击处理的肿瘤细胞(LNT)可以保护溶瘤病毒免受快速中和和消除。表面配体和受体,包括CD44和E-Cadherin,以及由于微米级尺寸而增强的肺毛细血管阻滞,促进了LNT-Ad11在转移病灶中的积聚。通过这种方式,与直接注射未经特殊处理的溶瘤病毒相比,LNT-Ad11在肺转移肿瘤中获得了110倍以上的富集,受益于Ad11的局部富集,肿瘤进展被抑制,免疫反应也被增强。总的来说,该研究开发了一种病毒隐藏的肿瘤靶向策略,使溶瘤病毒通过全身给药递送到肺转移肿瘤中。溶瘤病毒可以主动感染、内化、隐身于肿瘤细胞内,然后对肿瘤细胞进行液氮冲击处理,消除其致病性。这种类似特洛伊木马的载体避免了血液中的病毒中和和清除,促进了向肿瘤部位靶向传递。https://doi.org/10.1002/adma.202212210