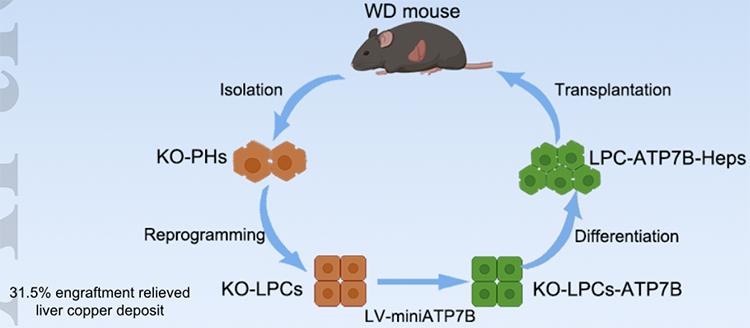
威尔逊病 (WD,也称为肝豆状核变性) 是一种罕见的遗传性疾病,由于 ATP7B 基因突变,导致病理性铜储存主要在肝脏和神经系统中。肝细胞移植显示出治疗潜力,然而,这种策略经常受到优质供体细胞短缺和同种异体免疫排斥的阻碍。2022年3月27日,上海交通大学王晓平团队在Hepatology (IF=17)在线发表题为“ATP7B gene therapy of autologous reprogrammed hepatocytes alleviates copper accumulation in a murine model of Wilson’s disease”的研究论文,该研究通过用小分子重编程来自 ATP7B −/− 小鼠的肝细胞,收获足够的肝祖细胞 (LPC),这些小分子在体外表现出很强的增殖和肝分化能力。在慢病毒介导的 miniATP7B 基因转染和再分化后,开发了功能性 LPC-ATP7B-Heps。RNA-seq数据显示,与LPC-GFP-Heps相比,LPC-ATP7B-Heps基因富集主要集中在氧化应激和细胞凋亡通路中,在高铜胁迫下的LPC-ATP7B-Heps中铜离子结合和细胞增殖通路富集。LPC-ATP7B-Heps 移植到 ATP7B−/− 小鼠中可减轻过量肝铜的沉积及其相关的炎症和纤维化,这与移植后四个月使用正常原代肝细胞观察到的情况相当。总之,该研究建立了一个新的自体重编程WD肝细胞系统,并在体外实现了ATP7B基因治疗。LPC-ATP7B-Heps 移植在 WD 小鼠模型中证明了对铜稳态的治疗效果。
威尔逊病 (WD)也称为肝豆状核变性,是一种与 ATP7B 基因(一种主要在肝细胞中表达的铜转运 ATP 酶)中的隐性致病变异相关的先天性疾病。WD 中铜向胆汁的运输受损导致铜在肝脏中的病理性积累,然后在大脑中积累。早期疾病检测、识别和治疗可防止 WD 的进展。药物干预(如锌盐和铜螯合剂)可减少病理性铜沉积,但无法恢复正常的铜代谢。原位肝移植是 WD 的有效治疗方法,但供体器官短缺和终生免疫抑制的需求限制了其应用。因此,迫切需要专注于恢复受影响 WD 患者体内铜稳态的替代疗法。基于细胞的治疗已成为挽救代谢性肝病的一种替代方法。当内源性细胞被破坏时,移植的肝细胞可以存活并强劲增殖,重新填充肝脏并发挥正常的肝功能 。来自未受影响个体的原代肝细胞 (PHs) 被认为是移植的最佳细胞类型,正如将正常大鼠 PHs 输送到 LEC 大鼠中的效果所证明的那样,WD 的啮齿动物模型消除了肝铜并逆转了疾病。尽管具有治疗潜力,但 PH 不能在体外增殖,并且新鲜分离的 PH 会迅速失去其肝脏基因表达特征。鉴于此,进行了几项研究,重点关注体外肝细胞扩增 。先前的报道还表明,通过小分子诱导,小鼠和人类 PH 可以转化为管状肝祖细胞 (LPC),这些肝祖细胞表现出细胞增殖和分化为功能性肝细胞的潜力。然而,一些缺点仍然存在,包括同种异体移植物之间的免疫反应和伦理问题。因此,来自WD动物或患者的自体重编程肝细胞的基因治疗成为潜在的选择。先前的数据表明,慢病毒介导的 ATP7B 在来自 WD 患者的 iPSC 分化的 HLC 中过表达或 ATP7B 基因转移到来自 LEC 大鼠的骨髓间充质干细胞 (BM-MSC) 中的可行性。两者都被证明可以降低细胞或大鼠肝脏中的铜负荷。为了实现这一点,通过修改早期建立的重编程协议对来自 ATP7B −/− 小鼠的 PH 进行重编程以生成 LPC。该研究发现肝细胞重编程和扩增培养基 (HREM) 显著促进 LPC 扩增至 40 多代。在 ATP7B 过表达后,重新分化的 LPC-ATP7B-Heps 能够重新填充 ATP7B −/− 小鼠的肝脏,减少肝铜的积累。因此,LPC-ATP7B-Heps 显示出治疗潜力,其结果可为开发 WD 和类似肝脏遗传疾病的新疗法铺平道路。https://aasldpubs.onlinelibrary.wiley.com/doi/10.1002/hep.32484