控制复制起点选择和激活的基于染色质的规则仍有待阐明。人们认为 DNA 复制从开放的染色质结构域开始。因此,复制起点位于开放和活跃的染色质中。
2022年4月13日,北京大学尚永丰及杨笑菡共同通讯在Signal Transduction and Targeted Therapy(IF=18)在线发表题为“LSD1 is required for euchromatic origin firing and replication timing”的研究论文,该研究报告了赖氨酸特异性去甲基化酶 1 (LSD1),它在生物化学上催化有利于染色质凝聚的 H3K4me1/2 去甲基化,与人类细胞中的 DNA 复制机器相互作用。该研究发现 LSD1 水平在 S 期早期达到峰值,通过促进常染色区域的复制起始点激发来进行 DNA 复制。事实上,富含 H3K4me2 的常染色质区是复制前复合物 (pre-RC) 结合的首选位点。值得注意的是,LSD1 缺乏导致全基因组复制从早期到晚期的转换。
该研究表明,LSD1 参与的 DNA 复制在机械上与将 TopBP1 相互作用检查点和复制调节器 (TICRR) 加载到 pre-RC 上以及随后在起源触发期间招募 CDC45 相关联。总之,这些结果揭示了 LSD1 在常染色质复制起始点激发和复制时间中的意外作用,突出了表观遗传调控在复制起始点激活中的重要性。由于 LSD1 的选择性抑制剂正被用作潜在的癌症治疗药物,该研究支持利用适当水平的 LSD1 来抑制抗 LSD1 治疗的副作用的重要性。
另外,2021年11月3日,北京大学尚永丰及孙露洋共同通讯在Signal Transduction and Targeted Therapy (IF=18.19)在线发表题为“The existence of a nonclassical TCA cycle in the nucleus that wires the metabolic-epigenetic circuitry”的研究论文,该研究报告了对细胞核中非经典 TCA 循环(nTCA 循环)的鉴定。该研究发现所有与 TCA 循环相关的酶(除了琥珀酸脱氢酶 (SDH)外)包括柠檬酸合酶 (CS)、乌头酸酶 2 (ACO2)、异柠檬酸脱氢酶 3 (IDH3)、酮戊二酸脱氢酶 (OGDH)、琥珀酰辅酶 A 合成酶 (SCS)、延胡索酸水合酶 (FH)和苹果酸脱氢酶 2 (MDH2)存在于细胞核中。该研究发现这些核酶催化不完整的 TCA 循环,类似于在蓝藻中发现的循环。该研究建议实施 nTCA 循环主要是为了产生/消耗代谢中间体,而不是用于能量生产。该研究证明了 nTCA 循环与染色质动力学和转录调控有着内在的联系。总之,该研究揭示了细胞核中非经典 TCA 循环的存在,该循环将代谢途径与表观遗传调控联系起来。

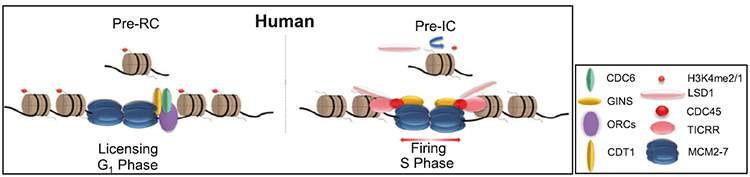
DNA 复制从被称为真核细胞复制起点的多个位点开始。尽管最近在对起源规范的理解方面取得了进展,但在高等真核生物中没有发现具有复制起源预测值的共有序列。而且,在每个细胞周期中,只有一部分复制起点用于复制真核基因组;非活性起源在正常条件下很少使用,但可能在特定的细胞程序或细胞微环境中被激活,这表明起源规范中的表观遗传调控。复制启动分两步进行:“许可”和“触发”。复制起点的许可从起始识别复合物 (ORC1-6) 的募集开始,并在 G1 期在细胞分裂控制蛋白 6 (Cdc6) 和细胞分裂周期 10 依赖性转录物 1 (Cdt1) 介导的加载将微型染色体维持 (MCM) 复合物转移到起源上,形成复制前复合物 (pre-RC)。随着细胞进入 S 期,通过将拓扑异构酶 II 结合蛋白 1 (TopBP1)、TopBP1 相互作用检查点和复制调节剂 (TICRR,也称为 Treslin)、细胞分裂周期蛋白 45 (CDC45) 和 GINS 募集到 pre-RC,复制起始点被激发。哺乳动物基因组的复制需要连续激活 30,000-50,000 个起始点,平均间隔为 100kb 的 DNA。一般来说,常染色区域富含在 S 期早期激发的起始点,而异染色区域则具有较晚激发的起始点。近年来,越来越多的证据表明表观遗传机制在复制起始点激发的时间和效率方面发挥着重要作用。表观遗传可塑性和染色质构型的改变允许产生适当的染色质环境,促进 ORC 和/或pre-RC的加载,从而促进随后的复制起始点激发。事实上,ORC 存在于对 DNase I 敏感的开放染色质中,并且经常与以活性组蛋白修饰为标志的启动子和增强子相关联,例如 H3K27ac、H3K9ac 和 H3K4me1/2。文章模式图(图源自Signal Transduction and Targeted Therapy )
据报道,组蛋白 H3 和 H4 的乙酰化加速了复制起始点激发或增加了 S 期复制起始点激发的效率。尽管 H3K4me2 与复制因子直接或间接募集到起点有关,但其在哺乳动物 DNA 复制中的作用和调节仍有待阐明,并且在特定基因座控制起始点选择和激活的基于染色质的规则仍有待描述。此外,赖氨酸特异性去甲基化酶 1 (LSD1) 被表征为催化 H3K4 去甲基化的胺氧化酶,此后主要在转录调控中进行研究。事实上,LSD1 构成了许多辅助抑制复合物,包括 CoREST、 CtBP 和 NuRD。然而,LSD1 在 DNA 复制中的作用尚不清楚。在该研究中,发现LSD1 在细胞周期的 DNA 合成阶段与 DNA 复制机器物理相关。该研究表明LSD1 参与常染色质区域的早期复制。该研究发现富含 H3K4me2 的区域是前 RC 结合的首选位点,并且LSD1 催化的 H3K4me2 去甲基化是通过促进 TICRR 与 pre-RC 的结合以及随后加载起始蛋白 CDC45 来进行复制起始点激发所必需的。总之,该研究表明 LSD1 缺乏导致全基因组从复制时间的早期到晚期的转换。https://www.nature.com/articles/s41392-022-00927-x