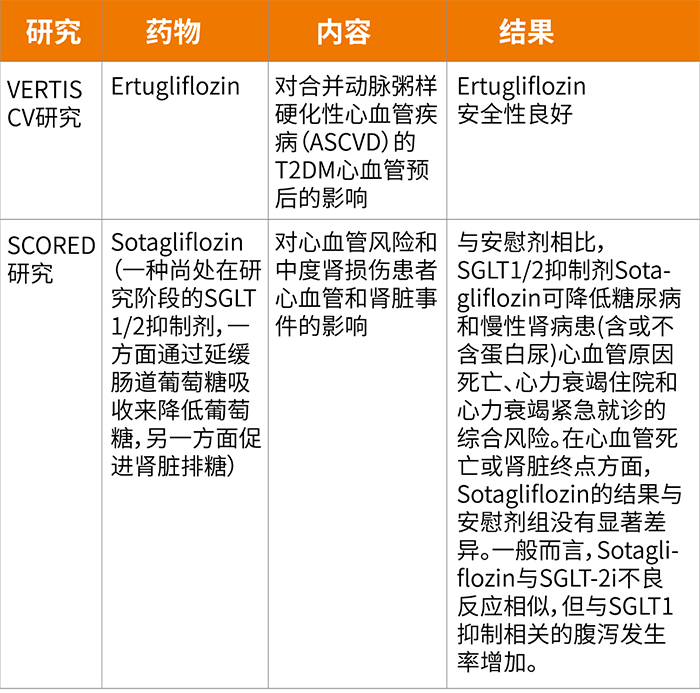
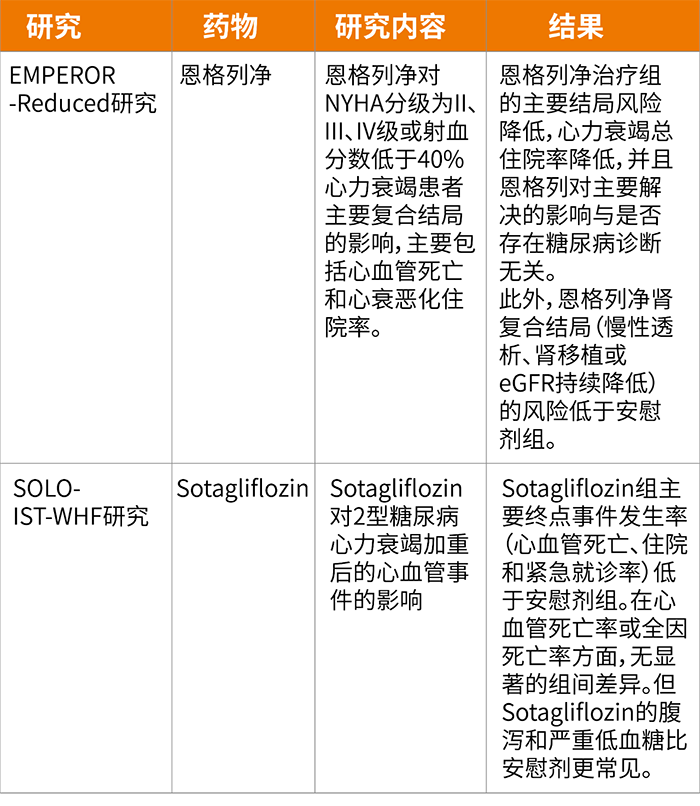
随着糖尿病领域新研究、新技术及新治疗的不断涌现,糖尿病管理策略也在不断更新。自2018 年以来,美国糖尿病协会(ADA)指南不再每年更新1次,而是随着新证据出现或新药获批,随时在网上进行动态更新。近期就对糖尿病诊断及分型、心血管疾病和风险因素管理及微血管病变和糖尿病足管理3个部分内容的证据进行了动态更新。在1型糖尿病的部分,针对1型糖尿病风险人群筛查的相关建议进行了修改,既往建议使用一组胰岛自身抗体对1型糖尿病风险人群及1型糖尿病一级亲属进行筛查,基于新证据的出现,将胰岛自身抗体具体为应用谷氨酸脱羧酶抗体(GAD)进行筛查。同时在这部分内容的最后加入新药证据的内容,具体如下:自2019年报道了在1型糖尿病高风险亲属中应用抗CD3抗体teplizumab具有明显的延缓1型糖尿病进展的作用[1]以来,2021年进行了进一步的研究[2]。目前这些数据已提交给美国食品和药物管理局(FDA),用于延缓或预防高危人群的1型糖尿病的发生,尽管该药物和其他同类药物目前都没有用于临床。在心血管疾病及风险管理部分,纳入了几项钠-葡萄糖协同转运蛋白-2抑制剂(SGLT-2i)的心血管试验的证据,主要包括:Ertugliflozin对心血管结局的疗效和安全性的研究( VERTIS CV )[3]、Sotagliflozin 对有心血管风险和中度肾功能损害2型糖尿病患者心血管和肾脏事件的影响( SCORED ) 研究[4]、恩格列净对射血分数降低的慢性心力衰竭患者的影响 ( EMPEROR-Reduced )[5],以及Sotagliflozin 对2型糖尿病(T2DM)心力衰竭加重后的心血管事件的影响(SOLOIST-WHF)[5]。在SGLT-2i试验的单元, 主要介绍了VERTIS CV研究和 SCORED研究的数据(详细见表1)。在降糖和心衰的单元首先介绍了EMPEROR-Reduced的数据和SOLOIST-WHF研究结果,通过EMPEROR-Reduced的数据指出在已确诊为射血分数下降的心衰(HFrEF)T2DM患者中,建议使用一种SGLT-2i来预防心衰恶化,降低心血管死亡的风险。从伴和不伴有T2DM 的HFrEF患者的数据比较来看,改善心血管结局是这类药物的作用,似乎与降糖作用本身无关。关于SGLT-2i对急性失代偿性心力衰竭住院患者和射血分数保留的心衰(HFpEF)患者的影响数据正在不断更新,例举了SOLOIST-WHF研究结果进行说明(详细见表2)。这项研究最初目的是评估Sotagliflozin对HFpEF患者的影响,最终没有发现射血分数对治疗效果的影响。不得不说的是这项研究中纳入的HFpEF患者的比例相对较小(只有21%的患者射血分数大于50%),并且这项试验的提前终止限制了确定Sotagliflozin对HFpEF影响的能力。在微血管病变和足管理部分,对于慢性肾脏病降糖药物的应用,加入了慢性肾病患者 (DAPA-CKD) 研究数据[6],DAPA-CKD研究评估了在标准治疗(RAASi)基础上添加达格列净延缓疾病进展或降低死亡风险的效果,研究的主要终点为肾小球滤过率(eGFR)持续降低≥50%、进展为终末期肾脏疾病(ESRD)、出现心血管死亡或肾病死亡的复合终点;次要终点分别为肾脏特异性复合终点、心血管死亡或心衰住院复合终点、全因死亡。结果显示,与安慰剂比较,达格列净显著降低主要终点风险39%,显著降低肾脏特异性终点44%、心血管终点29%、全因死亡风险31%。无论是否伴有2型糖尿病,主要终点获益一致。此外,在心血管和血压单元,更新了新一代盐皮质激素受体拮抗剂finerenone 在减少糖尿病肾病的肾衰竭和疾病进展 ( FIDELIO-DKD ) 的研究[7],结果显示在标准治疗基础上,与安慰剂相比,finerenone显著减少肾脏复合终点事件达18%。具体而言,finerenone通过降低首次出现肾功能衰竭、估计的肾小球滤过率(eGFR)在至少4周内从基线水平持续降低≥40%、肾脏死亡复合风险,延缓了CKD进展。关键次要终点观察显示finerenone减少14%的心血管复合终点事件,心血管复合终点包括首次发生心血管死亡、非致死性心肌梗死、非致死性卒中、心衰住院的时间。基于这项证据的更新,删除了血管紧张素转化酶抑制剂(ACEI)联合盐皮质激素抑制剂联合需要长时间随访研究的阐述。
[1]Herold KC, Bundy BN, Long SA, et al.; Type 1 Diabetes TrialNet Study Group. An anti-CD3 antibody, teplizumab, in relatives at risk for type 1 diabetes [published correction appears in N Engl J Med 2020;382:586]. N Engl J Med 2019;381:603–613. DOI: 10.1056/NEJMoa1902226
[2]Sims EK, Bundy BN, Stier K, et al.; Type 1 Diabetes TrialNet Study Group. Teplizumab improves and stabilizes beta cell function in antibody-positive high-risk individuals. Sci Transl Med 2021;13:eabc8980. DOI: 10.1126/scitranslmed.abc8980
[3]Cannon CP, Pratley R, Dagogo-Jack S, et al.; VERTIS CV Investigators. Cardiovascular outcomes with ertugliflozin in type 2 diabetes. N Engl J Med 2020;383:1425–1435. DOI: 10.1056/NEJMoa2004967
[4]Bhatt DL, Szarek M, Pitt B, et al; SCORED Investigators. Sotagliflozin in patients with diabetes
and chronic kidney disease. N Engl J Med 2021;384:129–139. DOI: 10.1056/NEJMoa2030186
[5]Packer M, Anker SD, Butler J, et al.; EMPEROR-Reduced Trial Investigators. Cardiovascular
and renal outcomes with empagliflozin in heart failure. N Engl J Med 2020;383:1413–1424.
DOI: 10.1056/NEJMoa2022190
[6]Heerspink HJL, Stefansson BV, Correa-Rotter R, et al. Dapagliflozin in patients with chronic kidney disease. N Engl J Med 2020;383:1436–1446. DOI: 10.1056/NEJMoa2024816
[7]Filippatos G, Anker SD, Agarwal R, et al. Finerenone and cardiovascular outcomes in patients with chronic kidney disease and type 2 diabetes. Circulation 2021;143:540–552. DOI: 10.1161/CIRCULATIONAHA.120.051898